Ecografía a pie de cama para el diagnóstico de lesiones toracoabdominales en pacientes con un traumatismo cerrado
Resumen
Antecedentes
La ecografía a pie de cama (EPC) ha surgido como la modalidad de cribado preferida para un presunto traumatismo corporal en muchos departamentos de urgencias en el mundo. Su aplicación mejor conocida es la ecografía abdominal centrada en el traumatismo (FAST, por sus siglas en inglés). La tecnología está disponible en casi todos los lugares, se puede realizar durante la reanimación y no expone a los pacientes ni al personal a radiaciones. Aunque muchos autores han recalcado la alta especificidad de la EPC, su sensibilidad varió notablemente entre los estudios. Esta revisión intentó compilar la mejor evidencia actual acerca de la exactitud diagnóstica de los protocolos de imagenología con EPC en el contexto del traumatismo toracoabdominal cerrado.
Objetivos
Determinar la exactitud diagnóstica de la EPC para detectar y excluir el líquido libre, las lesiones de órganos, las lesiones vasculares y otras lesiones (p.ej. neumotórax), comparada con un estándar de referencia diagnóstico (es decir, la tomografía computarizada [TC], la imagenología de resonancia magnética [IRM], la toracoscopia o la toracotomía, la laparoscopia o la laparotomía, la autopsia, o cualquier combinación de las anteriores) en pacientes con traumatismo cerrado.
Métodos de búsqueda
Se realizaron búsquedas en Ovid MEDLINE (1946 hasta julio 2017) y Ovid Embase (1974 hasta julio 2017), así como en PubMed (1947 hasta julio 2017), empleando una literatura prospectivamente definida y una estrategia de recuperación de datos. También se examinó la Biblioteca Cochrane, Google Scholar y BIOSIS en busca de citas potencialmente relevantes, y se analizaron las listas de referencias de los artículos de texto completo en busca de artículos omitidos por la búsqueda electrónica. Se realizó una búsqueda ampliada el 6 de diciembre de 2018 y se identificaron ocho nuevos estudios que se pueden incorporar a la primera actualización de esta revisión.
Criterios de selección
Se evaluaron los estudios para determinar su elegibilidad utilizando criterios de inclusión y exclusión predefinidos. Se incluyeron estudios diagnósticos de cohortes, prospectivos o retrospectivos, que reclutaron pacientes de cualquier edad y sexo que sufrieron cualquier tipo de lesión cerrada en un escenario civil. Los estudios elegibles tenían que proporcionar información suficiente para elaborar una tabla 2 x 2 de la exactitud diagnóstica y permitir el cálculo de la sensibilidad, la especificidad y otros índices de exactitud de la prueba diagnóstica.
Obtención y análisis de los datos
Dos autores de la revisión examinaron de manera independiente los títulos, los resúmenes y los textos completos de los informes mediante un formulario de extracción de datos preespecificado. La calidad metodológica de los estudios individuales se calificó mediante el instrumento QUADAS‐2 (la versión revisada y actualizada de la lista de ítems de la Quality Assessment of Diagnostic Accuracy Studies). Se calcularon la sensibilidad y la especificidad con los intervalos de confianza (IC) del 95%, se tabularon los pares de sensibilidad y especificidad con los IC y se mostraron en diagramas de bosque pareados mediante Review Manager 5 (RevMan 5). Para agrupar los cálculos resumidas de la sensibilidad y la especificidad e investigar la heterogeneidad entre los estudios se ajustó un modelo de dos variables mediante Stata 14.0.
Resultados principales
En esta revisión, se incluyeron 34 estudios con 8635 participantes. Las estimaciones resumidas de la sensibilidad y la especificidad fueron 0,74% (IC del 95%: 0,65% a 0,81%) y 0,96% (IC del 95%: 0,94% a 0,98%). Las razones de verosimilitud negativa y positiva agrupadas fueron 18,5 (IC del 95%: 10,8 a 40,5) y 0,27 (IC del 95%: 0,19 a 0,37), respectivamente. Hubo heterogeneidad apreciable entre los estudios, y la exactitud informada de la EPC dependió en gran medida de la población y el área corporal afectada. En los niños, la sensibilidad agrupada de la EPC fue 0,63 (IC del 95%: 0,46 a 0,77), en comparación con 0,78 (IC del 95%: 0,69 a 0,84) en la población de adultos o mixta. La especificidad asociada en los niños fue 0,91 (IC del 95%: 0,81 a 0,96) y en la población de adultos o mixta fue 0,97 (IC del 95%: 0,96 a 0,99). Para el traumatismo abdominal, la EPC tuvo una sensibilidad de 0,68 (IC del 95%: 0,59 a 0,75) y una especificidad de 0,95 (IC del 95%: 0,92 a 0,97). Para las lesiones de tórax, la sensibilidad y la especificidad fueron 0,96% (IC del 95%: 0,88% a 0,99%) y 0,99% (IC del 95%: 0,97% a 1,00%). Si se consideran los resultados de los 34 estudios incluidos en una población virtual de 1000 pacientes, según la mediana de la prevalencia observada (probabilidad previa a la prueba) de traumatismo toracoabdominal del 28%, la EPC pasaría por alto a 73 pacientes con lesiones e indicaría falsamente la presencia de lesiones en otros 29 pacientes. Además, en una población virtual de 1000 niños, según la mediana de la prevalencia observada (probabilidad previa a la prueba) de traumatismo toracoabdominal del 31%, la EPC pasaría por alto a 118 niños con lesiones e indicaría falsamente la presencia de lesiones en otros 62 niños.
Conclusiones de los autores
En pacientes con presunto traumatismo toracoabdominal cerrado, los resultados de una EPC positiva son útiles para guiar las decisiones terapéuticas. Sin embargo, con respecto al traumatismo abdominal, un examen negativo por EPC no descarta las lesiones y debe ser comprobado con una prueba de referencia como la TC. Lo anterior es de especial importancia en el traumatismo pediátrico, en el que la sensibilidad de la EPC es deficiente. Sobre la base del número pequeño de estudios en una población mixta, la EPC puede tener una sensibilidad mayor en las lesiones de tórax. Este hecho justifica ensayos más grandes para confirmar la exactitud de la EPC para diagnosticar el traumatismo torácico.
Resumen en términos sencillos
¿Cómo de exacta es la ecografía a pie de cama para el diagnóstico de las lesiones en el abdomen o el tórax en pacientes con traumatismo cerrado?
Antecedentes y objetivos
Los pacientes que sufren un accidente de tránsito o caen desde una altura tienen riesgo de traumatismo corporal cerrado (es decir, traumatismo no penetrante) y traumatismos múltiples. Los profesionales médicos que atienden a estos pacientes en el hospital necesitan conocer si los órganos vitales o los vasos están lesionados, y si hay cualquier hemorragia grave que requiera intervención inmediata. La ecografía a pie de cama (EPC), una forma de ecografía, es una técnica de imagenología portátil, no invasiva y que no conlleva radiaciones, que puede utilizarse en la cabecera del paciente. Se utiliza con frecuencia para ayudar a diagnosticar las lesiones en el departamento de urgencias. Se examinó la mejor evidencia científica acerca de la exactitud de la EPC, es decir, su capacidad de identificar o excluir de manera correcta las lesiones, en comparación con otras pruebas diagnósticas. La tomografía computarizada, la laparotomía y la autopsia se consideraron adecuadas como pruebas comparativas contra las cuales medir la exactitud de la EPC.
Características de los estudios
Se buscaron los estudios desde el año en el que se publicó el primer trabajo acerca del uso de la ecografía para diagnosticar a los pacientes con traumatismo hasta el 15 de julio de 2017. Se consideraron 2296 registros y se incluyeron 34 estudios relevantes que involucraron a 8635 participantes en esta revisión. Los 34 estudios se publicaron entre 1992 y 2017, y el número de participantes en cada estudio varió de 51 a 3181. Diez estudios incluyeron solo niños, dos estudios solo adultos y los 22 estudios restantes incluyeron niños y adultos.
Calidad de la evidencia
En muchos estudios no se proporcionó información importante acerca de la selección de los participantes y la elección de las pruebas diagnósticas contra las cuales comparar la EPC. Por lo tanto, se calificó la calidad metodológica de la evidencia disponible principalmente como poco clara.
Resultados clave
La ecografía a pie de cama tuvo una sensibilidad (es decir, la capacidad para detectar a un paciente con la enfermedad) del 74% y una especificidad (es decir, la capacidad para excluir a un paciente sin la enfermedad) del 96%. La sensibilidad y la especificidad variaron considerablemente entre los estudios, lo que se debió en parte a las variaciones en las características de los estudios, los participantes y las lesiones. En los niños la sensibilidad y la especificidad de la EPC fueron menores que en las poblaciones de adultos o mixtas, lo que significa que la EPC fue menos capaz de identificar o descartar una lesión. Según estos resultados, es de esperar que entre 1000 pacientes de una población con edad mixta con un presunto traumatismo cerrado en el abdomen o el tórax, la EPC pasaría por alto a 73 pacientes con lesiones e indicaría falsamente la presencia de lesiones en 29 pacientes que no están afectados. Este resultado recalca la necesidad de la imagenología adicional en pacientes con traumatismos para los que la EPC no muestra una lesión (es decir, un resultado negativo), para comprobar si realmente no presentan lesión.
Conclusiones de los autores
Summary of findings
| Population | Patients of any age and gender who sustained any type of blunt injury in a civilian scenario | |||||||
| Setting | Clinical evaluation at hospitals of any care level | |||||||
| Index test | Point‐of‐care sonography (POCS) as the primary imaging tool | |||||||
| Reference standard | Computed tomography (CT), magnetic resonance imaging (MRI), laparotomy, laparoscopy, thoracotomy, thoracoscopy, autopsy | |||||||
| Findings |
| |||||||
| Limitations |
| |||||||
| No. of participants (studies) | Summary sensitivity (95% CI) | Summary specificity (95% CI) | Summary LR+ (95% CI) | Summary LR‐ (95% CI) | Positive predictive value (95% CI) | Negative predictive value (95% CI) | Consequences in a virtual cohort of 1000a | |
| Missed injuries | Overtreated | |||||||
| 8635 (34) | 0.74 (0.65 to 0.81) | 0.96 (0.94 to 0.98) | 18.5 (10.8 to 40.5) | 0.27 (0.19 to 0.37) | 0.88 (0.81 to 0.94) | 0.90 (0.87 to 0.93) | 73 (If 280 people suffer an injury through trauma, 207 will be identified as injured, and 73 will be missed.) | 29 (If 720 people do not suffer an injury through trauma, 29 will be treated as though they had been injured, i.e. overtreated.) |
| Sensitivity analysis with a children‐only cohort | ||||||||
| 1384 (10) | 0.62 (0.47 to 0.75) | 0.91 (0.81 to 0.96) | 6.9 (2.5 to 18.8) | 0.42 (0.26 to 0.65) | 0.76 (0.53 to 0.89) | 0.84 (0.77 to 0.90) | 118 (If 310 children suffer an injury through trauma, 192 will be identified as injured, and 118 will be missed.) | 62 (If 690 children do not suffer an injury through trauma, 62 will be treated as though they had been injured, i.e. overtreated.) |
| aThe median prevalence was 28% for the complete study population and 31% for the children‐only cohort. | ||||||||
| Abbreviations CI: confidence interval | ||||||||
| Investigation of heterogeneity | Number of studies | Summary sensitivity (95% CI) | Summary specificity (95% CI) | Chi2a | P valueb |
| Reference standard | |||||
| Single CT | 25 | 0.75 (0.63 to 0.84) | 0.97 (0.93 to 0.98) | 0.18 (overall) | 0.9160 (overall) |
| CT plus laparotomy | 7 | 0.73 (0.58 to 0.84) | 0.95 (0.87 to 0.98) | ||
| Target condition | |||||
| Limited to free fluid/free air | 22 | 0.78 (0.68 to 0.85) | 0.97 (0.96 to 0.99) | 9.10 (overall) 0.06 (sensitivity) 8.08 (specificity) | 0.0106 (overall) 0.8100 (sensitivity) 0.0045 (specificity) |
| Free fluid/free air and organ injuries/vascular lesions | 7 | 0.80 (0.73 to 0.85) | 0.88 (0.70 to 0.96) | ||
| Age of participant | |||||
| Children | 10 | 0.63 (0.46 to 0.77) | 0.91 (0.81 to 0.96) | 7.32 (overall) 54.91 (sensitivity) 19.88 (specificity) | 0.0258 (overall) 0.0000 (sensitivity) 0.0000 (specificity) |
| Adults/mixed | 24 | 0.78 (0.69 to 0.84) | 0.97 (0.96 to 0.99) | ||
| Type of injury | |||||
| Abdominal injury | 27 | 0.68 (0.59 to 0.75) | 0.95 (0.92 to 0.97) | 17.36 (overall) 13.22 (sensitivity) 5.39 (specificity) | 0.0002 (overall) 0.0003 (sensitivity) 0.0202 (specificity) |
| Thoracic injury | 4 | 0.96 (0.88 to 0.99) | 0.99 (0.97 to 1.00) | ||
| aLarge values of the Chi2 statistic indicate that test performance may be associated with the particular covariate. bP values < 0.05 indicate statistical evidence that sensitivity and/or specificity differ between the examined groups. | |||||
| Abbreviations CI: confidence interval | |||||
Antecedentes
Enfermedad de interés diagnosticada
El traumatismo, incluido el traumatismo múltiple (definido por una Injury Severity Score [ISS] ≥ 16 o, según la nueva definición de Berlín, mediante una Abbreviated Injury Scale (AIS) ≥ tres para dos o más regiones corporales diferentes y una o más variables adicionales de cinco parámetros fisiológicos) (Pape 2014), aún es una causa principal de muerte y discapacidad en el mundo. El traumatismo grave es resultado principalmente de los accidentes de tránsito y de las caídas desde una altura. En 2010, según los datos del Global Burden of Disease Project de la Organización Mundial de la Salud (OMS), los accidentes de coche se clasificaron octavos en la mortalidad global (Lozano 2012) y décimos en todas las fuentes de años de vida ajustados en función de la discapacidad (Murray 2012). La campaña Década de Acción para la Seguridad Vial de 2011 a 2020 de la OMS y las Naciones Unidas se lanzó para fomentar la sensibilización acerca de esta inquietud de la salud pública e implementar medidas de prevención primaria sencillas y efectivas.
En la actualidad está en marcha una estrategia de "tratar primero lo que mata primero" en la mayoría de los centros traumatológicos de todo el mundo, apoyada por algoritmos estandarizados de gestión como el Advanced Trauma Life Support (ATLS). Los pasos clave de estos algoritmos son (Chapleau 2013):
-
mantener las vías respiratorias y establecer una oxigenación suficiente (es decir, mediante la intubación y la toracostomía con sonda en el caso de pneumo o hematotórax);
-
detener la hemorragia traumática (p.ej. mediante torniquetes en las extremidades, fajas pelvianas y fijadores externos, control quirúrgico o intervencionista de la hemorragia, aplicación de antifibrinolíticos como el ácido tranexámico y transfusión de productos sanguíneos, principalmente factores de la coagulación).
Los datos del German Trauma Registry indican una mortalidad general del 10% en los pacientes con lesiones graves tratados dentro de las redes traumatológicas organizadas y en los centros traumatológicos de gran volumen (German Trauma Society 2014). Puede haber un umbral biológico para la supervivencia del traumatismo que no pueda ser superado con cualquiera de las modalidades de tratamiento disponibles en la actualidad, y se necesitan esfuerzos adicionales de investigación translacional para lograr un cambio en el futuro. Aparte de las lesiones cerebrales no recuperables y las lesiones de la columna cervical superior, las principales causas de muerte prematura en el traumatismo múltiple son las lesiones del tórax y la hemorragia abdominal y retroperitoneal (Pfeifer 2016). La presencia de líquido libre alrededor del hígado o el bazo, los desgarros capsulares, las contusiones o laceraciones de órganos y las lesiones vasculares influyen en las tomas de decisiones tempranas en el traumatismo grave.
Los apuñalamientos (por instrumentos afilados, o armas como los cuchillos) y los disparos de arma de fuego se asocian con altas probabilidades de lesión a órganos o vasos. La ubicación diferenciada de las heridas puede orientar hacia un traumatismo significativo en los pulmones, el corazón, el mediastino, el hígado, el bazo y la aorta torácica o abdominal. La calidad y la cantidad de lesiones sufridas en los ámbitos civiles y los conflictos armados difieren en muchos aspectos (p.ej. según el tipo de arma, pistola o bala, la balística de la herida, la armadura protectora, el ambiente austero [es decir, en el que la atención médica se proporciona bajo condiciones que no llegan a ser óptimas desde el punto sanitario ni hospitalario] y otros). La mayoría de los pacientes con traumatismo penetrante necesitan exploración quirúrgica inmediata (específicamente en el caso de inestabilidad hemodinámica), y la imagenología preoperatoria tiene una función más bien complementaria en esta situación.
Sin embargo, en el traumatismo cerrado la imagenología radiográfica es una parte inevitable del examen clínico. La exploración física puede mostrar signos indirectos de lesión interna (p.ej. marcas de contusión), pero estos signos no son consistentes, sensibles ni específicos. La tomografía computarizada (TC) se considera la técnica estándar de imágenes en el servicio de urgencias y actualmente también es la prueba diagnóstica de referencia indiscutible en el escenario del traumatismo. Si los pacientes se trasladan de inmediato al quirófano antes de realizar la imagenología con TC, la laparotomía de urgencia, la laparoscopia o la toracotomía son el estándar de referencia preferido. Si los pacientes mueren en el departamento de urgencias antes de poder realizar cualquier procedimiento imagenológico o quirúrgico, el diagnóstico definitivo se obtiene durante la autopsia patológica o forense. No obstante, la ecografía a pie de cama (EPC) se puede realizar durante la reanimación, repetirse en cualquier lugar y cualquier momento que se necesite y no incluye exposición a radiaciones.
La ecografía a pie de cama ha surgido como una parte integrante de los algoritmos del traumatismo y es la modalidad de cribado inicial preferida para la hemorragia toracoabdominal en la mayoría de las regiones del mundo. Como cualquier otro procedimiento de imagenología o prueba diagnóstica utilizada con fines de cribado, es importante comprobar que:
-
un resultado negativo de la prueba índice sea fiable para excluir la afección de interés (garantizar que los episodios de inestabilidad hemodinámica durante la cirugía de descompresión cerebral o la fijación de las fracturas de la columna, la pelvis o el fémur no son causadas por una hemorragia grave súbita abdominal, torácica o retroperitoneal);
-
un resultado positivo de la prueba índice es fiable para probar la afección de interés (por lo tanto, se minimiza el número de toracotomías y laparotomías negativas o innecesarias, o sus equivalentes mínimamente invasivos).
Los resultados falsos negativos y falsos positivos de la EPC pueden confundir a los equipos de traumatología y perjudicar las prioridades de atención.
La exactitud diagnóstica (o eficacia) es el primer nivel de la jerarquía de Thornbury Fryback de la evaluación de la utilidad de un procedimiento de prueba diagnóstica (Fryback 1991). Aunque el valor y la utilidad de cierta prueba no se pueden derivar solo de su exactitud, sería absurdo examinar la efectividad o la eficiencia de una prueba diagnóstica poco exacta.
Por lo tanto, determinar la exactitud es el primer paso imprescindible en la evaluación de tecnologías sanitarias de la EPC. Esta revisión intentó generar la mejor evidencia disponible acerca de la exactitud diagnóstica de los protocolos clínicos de imagenología por ecografía en el contexto del traumatismo toracoabdominal y múltiple, en comparación con estándares de referencia apropiados. Guiará a los clínicos con respecto a la probabilidad de las lesiones de tórax y abdominales según ciertas probabilidades a priori y los resultados de la ecografía, y puede facilitar la decisión de realizar una tomografía computarizada o programar a los pacientes para laparoscopia o laparotomía de urgencia, u otros procedimientos intervencionistas.
Debido a la posible (mayor) utilidad y valor de la EPC en el traumatismo cerrado en comparación con el penetrante, esta revisión solo consideró los estudios originales que incluyeron participantes con lesiones cerradas, o en una población mixta siempre que se proporcionaran detalles suficientes para explorar la exactitud de la EPC en este grupo.
Otro aspecto que requiere un examen cuidadoso es el uso de la EPC en los algoritmos de traumatismo pediátrico. Los niños son vulnerables a la radiación con fines diagnósticos, y el riesgo atribuible para toda la vida (RATV) de cáncer debido a la imagenología médica debe mantenerse al mínimo necesario. Aun así, puede haber situaciones en las que afecciones agudas y potencialmente mortales requieren de la emisión de radiaciones (es decir, tomografía computarizada de hilera multidetectora [TCHM]), en lugar de las técnicas de imagen sin radiación (p.ej. la EPC o la imagen por resonancia magnética [IRM]).
Prueba/s índice
La ecografía ha surgido como la técnica estándar de imagen de cabecera en los servicios de urgencias de todo el mundo. El progreso tecnológico ha dado lugar a que existan equipos cada vez más ligeros y móviles (es decir, portátiles) (también disponibles en el contexto preclínico, p.ej. en helicópteros o vehículos de rescate). Los progresos adicionales incluyen el dúplex color, la técnica de imagen mejorada por contraste e incluso la exploración tridimensional (3D).
En el contexto del traumatismo, la EPC se realiza con frecuencia como ecografía abdominal centrada en el traumatismo (FAST, por sus siglas en inglés) (Scalea 1999). En su forma básica, la FAST incluye vistas oblicuas de los cuadrantes abdominales superior izquierdo, superior derecho, inferior izquierdo e inferior derecho, así como un examen sagital del abdomen medio y una vista transversal de la región pelviana. El objetivo clave del examen FAST original es detectar el líquido libre, como un substituto de sangre o de hemorragia activa.
El FAST original se ha modificado y complementado en muchos aspectos. Las extensiones más útiles y técnicamente sencillas fueron el examen en busca de hematotórax (mediante planos oblicuos o intercostales, o ambos) y, mediante una vista del xifoides, para la efusión pericárdica. La ecografía a pie de cama también ha resultado ser fiable para detectar el neumotórax (Blaivas 2005). Los examinadores capacitados podrían mostrar y calificar la lesión de los órganos abdominales, aunque es probable que lo anterior exceda los límites diagnósticos de la EPC en la fase de reanimación temprana.
En esta revisión se ha utilizado el término EPC en lugar de FAST debido a las variaciones en las definiciones y las metas establecidas en diferentes centros y países. En la práctica clínica, la ecografía (o ultrasonografía) como técnica de imagen con frecuencia se abrevia y se denomina como ecografía. En conjunto, la evolución tecnológica de los equipos, el aumento de las habilidades de los operadores y los progresos significativos en la adquisición y el procesamiento de las imágenes han cambiado de manera significativa el criterio de los profesionales sanitarios acerca de la función de la ecografía en el contexto de los cuidados intensivos. La ecografía ha evolucionado de ser una herramienta de cribado aproximado a ser una modalidad de imagen concluyente.
Por lo tanto, la prueba índice para esta revisión fue cualquier aplicación clínica de la EPC realizada en el contexto del traumatismo cerrado, dirigida a detectar signos directos o indirectos de lesiones en la cavidad o el espacio torácico, abdominal o retroperitoneal y sus órganos y vasos.
Vía clínica
El examen clínico solo tiene poca (si es que alguna) función para excluir las lesiones torácicas o abdominales. La presencia de lesiones externas como las marcas del cinturón de seguridad puede aumentar la probabilidad de desgarros viscerales, pero su ausencia no excluye el traumatismo importante. En la actualidad todos los algoritmos de traumatismo grave incorporan la EPC toracoabdominal como una herramienta de imagenología. Sin embargo, la interpretación de las imágenes ecográficas depende de la experiencia y los antecedentes clínicos de los operadores individuales. Este componente subjetivo influye en la toma de decisiones e impide las comparaciones entre los exámenes iniciales y de seguimiento hechos por diferentes examinadores. En 2013, Van Vugt y colegas publicaron un protocolo de procedimientos basado en la evidencia para el traumatismo cerrado que ilustró los efectos beneficiosos de entrenar a los equipos de traumatología en EPC (FAST), en combinación con un curso de ATLS (Van Vugt 2013).
Prueba/s alternativa/s
En la actualidad la EPC es cuestionada debido al uso temprano y liberal de la TCHM, ya sea como TCHM abdominal, torácica, toracoabdominal o de todo el cuerpo. Esta última ha surgido como la modalidad de diagnóstico preferida en la mayoría de los centros traumatológicos europeos, y también se utiliza en los EE.UU. y otros países de ingresos altos. La denominada "exploración completa" comprende por lo general una TC craneal inicial, seguida de una TC mejorada por contraste de la base del cráneo hasta la pelvis o la región trocantérica. La TCHM de cuerpo entero es muy específica de manera que se minimizan los resultados falsos positivos (Stengel 2012), por lo que puede influir en las prioridades de atención según la regla "tratar primero lo que mata primero". Los datos del German Trauma Registry indican que la exploración completa mejora la supervivencia en las cohortes no seleccionadas de pacientes con traumatismo y hemodinámicamente inestables (Huber‐Wagner 2013). Sin embargo, hay inquietudes con respecto a la exposición excesiva a las radiaciones causada por el uso de la exploración completa en condiciones no críticas a nivel individual y poblacional (Asha 2012). Aunque los algoritmos de reconstrucción y procesamiento de la reducción de la dosis están disponibles, es un tema de debate si producen imágenes similares, en cuanto a calidad y certeza diagnóstica, a las producidas por los protocolos convencionales.
La exploración completa no solo es una herramienta a tomar en cuenta en las técnicas de imagen; también se considera el estándar de referencia diagnóstico con el que se deben comparar los resultados de la EPC. Lo anterior da lugar a un conflicto metodológico interesante, ya que será casi imposible comparar ambas modalidades de imagen de una manera directa en el escenario del traumatismo.
Fundamento
En los países de ingresos altos es dudoso si los hallazgos de la EPC afectan las decisiones de tratamiento en el traumatismo grave. Este hecho se puede ilustrar por los siguientes cuatro escenarios posibles.
-
La EPC es positiva para líquido libre abdominal o torácico, o ambos, en un paciente hemodinámicamente estable. Este hallazgo dará lugar a la realización de un examen por TC (por lo general una exploración completa) para identificar las fuentes de la hemorragia. En la mayoría de los casos, la transfusión hemostática (más la embolización arterial [ETA]) y la monitorización en la unidad de cuidados intensivos (UCI) será el tratamiento de elección en este contexto.
-
La EPC es negativa para el líquido libre abdominal o torácico, o ambos, en un paciente hemodinámicamente estable. Este hallazgo dará lugar a la realización de un examen por TC (por lo general una exploración completa) que compruebe que no hay una fuente de hemorragia activa que la ecografía pasó por alto.
-
La EPC es negativa para líquido libre abdominal o torácico, o ambos, en un paciente hemodinámicamente inestable. Este hallazgo casi siempre dará lugar a la realización de una TC (por lo general una exploración completa) para identificar las fuentes de hemorragia, y a la toma de decisiones acerca de la ETA o la cirugía de urgencia, o ambas.
-
La EPC es positiva para líquido libre abdominal o torácico, o ambos, en un paciente hemodinámicamente inestable. Actualmente es poco probable que no se pueda lograr la estabilidad mediante la reanimación hemostática y otros esfuerzos de cuidados intensivos para preparar a los pacientes para una exploración completa.
El escenario 4 es relevante, pero poco frecuente, en el mundo occidental. Hay pocas ocasiones en las que todos los esfuerzos de reanimación fracasan y los pacientes se programan para toracotomía o laparotomía de urgencia, o ambas, según los resultados de la EPC sola. Aun así, estas situaciones ocurren y las guías de práctica clínica deben incluir recomendaciones sobre cómo hacer frente a esta situación.
Sin embargo, en los países de ingresos medios y bajos la EPC (además de las radiografías convencionales) puede representar la herramienta de diagnóstico no invasiva más compleja o la única disponible para detectar la hemorragia traumática significativa y para guiar la selección de los pacientes. El terremoto de Sichuan en 2008, que mató a 69 197 personas y dejó 18 222 desaparecidos, fue un ejemplo clásico. La ecografía abdominal centrada en el traumatismo probó ser efectiva, eficiente y posiblemente salvó vidas bajo estas circunstancias excepcionales (Zhou 2012). Observaciones similares se hicieron después del terremoto en Haití en 2010. El terremoto de Nepal en abril de 2015 (que mató a más de 6000 personas y dejó a 2 800 000 sin hogar) demostró cómo la FAST puede desempeñar una función en la selección efectiva de los pacientes fuera del contexto de la investigación clínica.
Objetivos
Determinar la exactitud diagnóstica de la EPC para la detección y la exclusión de:
-
líquido libre en la cavidad torácica o abdominal;
-
lesiones de órganos con o sin hemorragia en la cavidad torácica o abdominal;
-
lesiones vasculares de la aorta torácica o abdominal, u otros vasos principales; y
-
otras lesiones (p.ej. neumotórax);
en comparación con los siguientes estándares de referencia diagnósticos: tomografía computarizada (TC; "exploración completa"), imagen por resonancia magnética (IRM), toracotomía, laparotomía, laparoscopia, toracoscopia, autopsia, o cualquier combinación de estas.
Objetivos secundarios
Los objetivos secundarios de esta revisión fueron investigar la influencia de las características de los estudios individuales y las cohortes como
-
el estándar de referencia;
-
la enfermedad de interés;
-
la edad de los pacientes (pediátricos versus no pediátricos);
-
el estado de la enfermedad de los pacientes: el tipo de traumatismo, el tipo de lesión, la estabilidad hemodinámica, la gravedad de la lesión o la probabilidad de supervivencia;
-
el ambiente;
-
la pericia y los antecedentes del operador;
-
el equipo;
-
los umbrales de la prueba;
sobre los exámenes positivos y negativos con la EPC.
Se proporcionan más detalles en la sección de la revisión Investigaciones de la heterogeneidad.
Métodos
Criterios de inclusión de estudios para esta revisión
Tipos de estudios
Se incluyeron:
-
estudios diagnósticos de cohortes, prospectivos o retrospectivos, que reclutaron pacientes con traumatismo cerrado:
-
sometidos a cualquier tipo de EPC como modalidad primaria de imagenología para detectar lesiones toracoabdominales; y
-
sometidos también a pruebas de referencia de imagen o invasivas predefinidas para verificar los resultados de la EPC;
-
-
estudios que proporcionaron tablas 2 x 2 (o información suficiente para tabular los resultados) para permitir el cálculo de la sensibilidad, la especificidad y otros índices de exactitud de la prueba diagnóstica.
Se excluyeron:
-
los estudios diagnósticos de casos y controles que compararon pacientes con un estado conocido de casos con controles saludables, ya que este diseño crea poblaciones artificiales y tiende a sobrestimar la sensibilidad de la prueba índice;
-
las series de casos clínicos y los informes de casos;
-
los estudios con pruebas índice o de referencia poco claras; y
-
los estudios que no permitieron la creación de tablas 2 x 2.
Participantes
La población objetiva de esta revisión incluyó pacientes de cualquier edad o sexo que sufrieron cualquier tipo de traumatismo cerrado en un escenario civil y fueron trasladados a un hospital de cualquier nivel de atención. Además, para ser elegibles los participantes tenían que haber sido sometidos a una EPC como herramienta primaria de imagen y haber sido seguidos como enfermos hospitalizados o ambulatorios con diferentes modalidades diagnósticas para verificar si la afección de interés estaba presente o ausente.
Debido a las diferencias claras en el tratamiento clínico, se excluyeron de manera deliberada los pacientes con lesiones penetrantes, así como los miembros de las Fuerzas Armadas heridos en el campo de batalla.
Pruebas índice
Cualquier tipo de EPC realizada en un contexto de traumatismo (p.ej. ecografía FAST del abdomen o el tórax, o ambos, o cualquier protocolo de ecografía avanzada) concebida para detectar:
-
líquido libre (como substituto de hemorragia) en el abdomen, el espacio retroperitoneal o el tórax;
-
lesiones a órganos sólidos como el hígado o el bazo (incluidos los intentos para calificar la gravedad);
-
lesiones de vasos principales; y
-
otras lesiones (p.ej. neumotórax, como indica la presencia de aire en el espacio pleural).
Las variaciones en la tecnología y la aplicación de la EPC (p.ej. especificación de las máquinas y las sondas de ecografía y cuán actualizadas estaban, así como el tratamiento de los resultados no concluyentes de la prueba) se abordan en la sección de la revisión Evaluación de la calidad metodológica. Se planificó examinar su posible influencia en los cálculos de la exactitud diagnóstica en la sección de la revisión Investigaciones de la heterogeneidad.
Enfermedades de interés
Esta revisión se centró en el traumatismo cerrado toracoabdominal y múltiple, que significa cualquier fuerza contusa y no penetrante al abdomen y el tórax y a las vísceras sólidas y huecas, así como a los vasos principales. Las afecciones objetivo consideradas en esta revisión incluyeron:
-
líquido libre en:
-
la cavidad torácica (uni o bilateral, cuando se especificó);
-
la cavidad abdominal (por cuadrante abdominal, cuando se especificó);
-
el espacio retroperitoneal;
-
el pericardio; o
-
el mediastino;
-
-
lesiones de órganos, definidas como:
-
lesiones hepáticas (p.ej. desgarros capsulares, hematoma, desgarros de tejidos);
-
lesiones esplénicas (p.ej. desgarros capsulares, hematoma, desgarros de tejidos);
-
lesiones a otros órganos sólidos (p.ej. páncreas, riñones);
-
lesiones a vísceras huecas; o
-
desgarros de cualquier otro órgano por ecografía;
-
-
lesiones vasculares, definidas como:
-
disección o rotura de la aorta torácica o abdominal, o ambas;
-
rotura de otros vasos como las arterias ilíacas;
-
-
otras lesiones (p.ej. neumotórax, indicado por la presencia de aire en el espacio pleural en la cavidad torácica).
Como parte de las Investigaciones de la heterogeneidad se analizó el efecto de los diferentes tipos de afecciones objetivo. Las afecciones objetivo se categorizan como substitutos de traumatismo cerrado (es decir, líquido libre y aire libre, llamada evaluación limitada), y signos substitutos y directos de daño a órganos (es decir, lesiones de órganos y lesiones vasculares, llamada evaluación completa).
Estándares de referencia
Para aceptarlo como un estándar de referencia diagnóstico, se debía especificar el uso deliberado (y el razonamiento para su uso) del método específico. Para evitar el sesgo de verificación, todos los participantes debían recibir un estudio por imagen o una prueba invasiva independientes, aparte del examen inicial con EPC.
Las siguientes pruebas se clasificaron como estándares de referencia para confirmar la presencia o ausencia de la afección objetivo:
-
cualquier tipo de tomografía computarizada de las cavidades corporales principales (es decir, tórax, abdomen, pelvis), selectiva o realizada como examen de todo el cuerpo. Se planificó estratificar los resultados para el uso de agentes de contraste intravenosos u orales, o ambos, y el intervalo entre la EPC y la TC;
-
cualquier tipo de IRM de las cavidades corporales principales;
-
laparotomía (mediante abordaje mediano o transversal) o laparoscopia, diagnóstica o terapéutica;
-
toracotomía (mediante abordaje por esternotomía mediana o clamshell) o toracoscopia, diagnóstica o terapéutica;
-
autopsia, hecha por patólogos o por forenses.
Métodos de búsqueda para la identificación de los estudios
We developed a reproducible search strategy in major online databases based on recommendations of the Cochrane Diagnostic Test Accuracy (DTA) Group and a systematic review performed previously (Stengel 2005). We sought assistance and advice from the Cochrane Injuries Group and its Information Specialist to create a search algorithm with high sensitivity. We also requested access to the Cochrane Injuries Group Specialised Register and searched the Cochrane Library for relevant studies included in published reviews. Furthermore, we used a snowball procedure to identify related articles and articles cited in the reference lists of individual publications, and used Google Scholar as an additional search tool.
Búsquedas electrónicas
We searched the following electronic sources.
-
Ovid MEDLINE (1946 to 15 July 2017).
-
PubMed (not MEDLINE) (1947 to 15 July 2017).
-
Ovid Embase (1974 to 15 July 2017).
Search strategies are shown in Appendix 1.
We performed a further search on 6 December 2018; details of the eight potentially relevant studies identified have been added to the Characteristics of studies awaiting classification and Studies awaiting classification sections, and may be incorporated into the review at the next update.
Búsqueda de otros recursos
A systematic review by Scherer and colleagues showed that results from studies that have not been published in a full‐text format are systematically different from fully published results (Scherer 2007). We therefore searched the BIOSIS database for conference abstracts to identify potentially relevant studies that had not yet been published in a journal format (see Appendix 1).
We planned to contact authors of individual studies by email, letter, or phone, if we considered their results to be important but needed further explanation or raw data. We guaranteed that any data exchange complied with the International Conference on Harmonisation Good Clinical Practice (ICH‐GCP) principles and rules and regulations of data safety and security.
Obtención y análisis de los datos
We employed standard operating procedures (SOP) for the selection of studies, data extraction, and recording. This included the following principles:
-
screening of titles, abstracts, and full texts of study reports identified by the search strategy by two review authors working independently;
-
use of a data extraction form (including individual study characteristics, individual patient profiles, definition of procedures, etc.);
-
dual assessment and data entry;
-
dual assessment of methodological quality of individual studies;
-
resolution of conflicts by a third review author.
This guarantees transparency and adherence to Cochrane standards and other recommendations (e.g. those issued by the EQUATOR (Enhancing the QUAlity and Transparency Of health Research) group).
Selección de los estudios
Two review authors (AH, JL) independently screened the titles and abstracts of the identified reports, documenting details of selected studies in a predefined electronic spreadsheet and assessing studies for eligibility in terms of the predefined inclusion and exclusion criteria. If it was not possible to make a decision based on title and abstract alone, the full texts of potentially relevant studies were assessed. Any disagreements between authors regarding the selection of studies were resolved by a third expert (DS). The study selection process is documented in a detailed flow chart (Figure 1).
Extracción y manejo de los datos
As stated above, we established an SOP for data extraction for systematic reviews, meta‐analyses, and health technology assessment (HTA) reports. We adhered to ICH‐GCP, Good Epidemiological Practice (GEP), and other relevant rules and recommendations. We have trained personnel on site to record, manage, and audit data, and our data storage modes comply with federal legislation on data safety for research purposes. Two review authors (AH, JL) independently extracted data from original papers in duplicate, and resolved discrepancies by discussion, moderated by a third review author (DS). They extracted the following information from published papers:
-
study characteristics (author, year of study, year of publication, journal reference, study design, inclusion/exclusion criteria, operator characteristics, hardware specifications, index test used, reference test used, general setting (urban/rural), mass casualty (yes/no));
-
patient characteristics (age, gender, type of trauma, type of injury, injury severity, haemodynamic stability, probability of survival);
-
outcome of the index test as assessed in the individual studies by diagnosing the target condition and, if available, the number of participants with inconclusive results or who had no test result;
-
diagnostic 2 x 2 tables, cross‐classifying the disease status on the basis of the reference test (i.e. number of true‐positive, false‐positive, false‐negative, and true‐negative results).
Diagnostic accuracy was expressed by individual and pooled indicators such as sensitivity and specificity with 95% confidence intervals (CI), positive and negative likelihood ratios (LR), positive predictive value (PPV), negative predictive value (NPV), and the summary receiver operating characteristic curve (SROC).
Evaluación de la calidad metodológica
Two review authors (AH, JL) independently used the QUADAS‐2 tool (the revised and updated version of the original Quality Assessment of Diagnostic Accuracy Studies list of items) to assess methodological quality of individual studies (Whiting 2011). Any discrepancies were resolved by discussion, moderated by a third review author (DS). QUADAS‐2 includes four main domains, namely: patient selection, index test, reference standard, and flow and timing. We assessed each domain with regard to risk of bias, rating them as 'low', 'high', or 'unclear'. We assessed concerns regarding applicability only for the first three domains, categorising them as 'low', 'high', or 'unclear'. Signalling questions were answered as 'yes', 'no', or 'unclear' (see also Appendix 2). By using tailored review‐specific signalling questions we were able to perform a custom‐made assessment of the methodological quality of all included studies. We omitted the signalling question "Was any case‐control design avoided?" in Domain 1: Patient selection since we did not include any case control study, case series, or case reports. We added three signalling questions to Domain 2: Index test and two signalling questions to Domain 3: Reference test referring to operator's expertise and background, technical features of the hardware, and appropriateness of the ultrasound protocol and reference imaging standard. In Domain 4: Flow and timing, we included the signalling question "Did all participants receive a reference standard?" in order to explore the risk of partial verification bias.
Análisis estadístico y síntesis de los datos
If at least one of the target conditions was detected (i.e. pneumothorax, free fluid, organ or vessel injury), we considered the patient (participant) to be traumatised or test‐positive. Otherwise, we considered the participant to be uninjured or test‐negative. Our observational unit of interest was thus the individual participant, not a particular injury, and we did not evaluate single target conditions separately in the primary analysis. We used inconclusive test results as reported in the primary studies. For individual studies, we calculated sensitivity and specificity with 95% CI, tabulated pairs of sensitivity and specificity with CI, and depicted estimates by coupled forest plots using Review Manager 5 (RevMan 5) (Review Manager 2014).
Due to the subjective nature of the interpretation of POCS findings, we expected implicit thresholds in test positivity. We assessed a possible threshold effect visually by plotting true‐positive rates (sensitivity) from each study against false‐positive rates (1 − specificity) in a receiver operating characteristic (ROC) space and coupled forest plots of sensitivity and specificity. Since the dichotomous operationalisation of the test result does not enable explicit thresholds, we used the bivariate model according to Reitsma 2005, which is a robust statistical model taking the underlying relationship between sensitivity and specificity into account. The random‐effects approach allows for calculating sensitivity and specificity estimates while controlling for heterogeneity across studies. We fitted the models in Stata (Stata 2017) using the 'metandi' command and produced SROC plots using RevMan 5. We estimated average sensitivities and specificities using the bivariate model. We obtained likelihood ratios post estimation using the parameters of the bivariate model (see Summary of findings table 1).
Investigación de la heterogeneidad
We assessed heterogeneity visually by inspecting the coupled forest plots and plots of study results in the SROC space. We also investigated possible sources of heterogeneity by adding single covariates to the basic bivariate random‐effects model. We conducted fitting of the bivariate model via the 'xtmelogit' command in Stata (Takwoingi 2016). We investigated the effect of adding covariates by conducting a likelihood ratio test that compared the ‐2 log likelihoods of the basic bivariate model to a model including a single covariate. If a significant reduction in the ‐2 log likelihood was detected (indicated by a P value of < 0.05), test performance was considered to be associated with the particular covariate. For statistically significant test results, we determined whether the covariate was associated with the estimated sensitivity, specificity, or both (Macaskill 2011), by removing the covariate terms for either sensitivity or specificity, and comparing the fit of each alternative model using likelihood ratio tests.
For tests of heterogeneity, we required a minimum of 10 studies in total and at least four studies per subgroup. We had to dichotomise the covariates we investigated, and differentiate between paediatric and non‐paediatric (i.e. adult/mixed populations), surrogates of injury (e.g. air, free fluid) and organ lacerations, abdominal injuries (i.e. injuries exclusively located in the abdomen) or chest injuries (i.e. injuries exclusively located in the chest), and single CT versus CT plus laparotomy used as reference standard (see Summary of findings table 2).
Análisis de sensibilidad
We performed sensitivity analyses to investigate how individual QUADAS‐2 key domains (i.e. patient selection, index test, reference standard, and flow and timing) affected accuracy estimates, and to explore whether the different evaluations of the two independent review authors within two original studies influenced pooled sensitivities or specificities, or both, of the index test. Moreover, we examined the impact of participants' age on accuracy estimates by only including paediatric studies.
Evaluación del sesgo de notificación
We did not assess reporting bias because there are no accepted ways of doing this for diagnostic test accuracy studies (Deeks 2005).
Results
Results of the search
We conducted the electronic search on 15 July 2017 in Ovid MEDLINE, PubMed, and Ovid Embase, applying the strategy shown in Appendix 1. We identified 2872 publications including 576 duplicates (Figure 1). After screening the titles or abstracts of 2296 records, 91 studies remained for further evaluation according to our predefined inclusion and exclusion criteria (Types of studies). After screening the full texts of these 91 studies, we discarded 57 and included 34. We regarded the published data as sufficient to answer our research questions and so did not require individual author contact.
Included studies
We extracted information from the 34 included studies according to predefined criteria (Characteristics of included studies). The included studies compared POCS to various imaging and surgical standards (i.e. CT, conventional radiography, laparotomy, thoracotomy, and autopsy) and were published between 1992, Tso 1992, and 2017, Calder 2017, with sample sizes ranging from 51 participants in Benya 2000 to 3181 in Becker 2010. Retrospective and prospective designs were equally distributed, and half of all investigations were conducted in the USA. Ten studies enrolled only children and adolescents, with the age of participants ranging from 1 to 18 years (Benya 2000; Calder 2017; Coley 2000; Corbett 2000; Emery 2001; Fox 2011; Menichini 2015; Soudack 2004; Valentino 2010; Zhou 2012). Two studies included only adults (Blaivas 2005; Verbeek 2014), and 22 studies enrolled participants of any age. Four studies addressed thoracic trauma exclusively (Blaivas 2005; Nandipati 2011; Ojaghi 2014; Zhang 2006). Half of all participants were admitted to level I trauma centres.
Excluded studies
Fifty‐five studies did not meet the inclusion criteria and were excluded (Characteristics of excluded studies). The main reasons for exclusion were insufficient information to allow for calculating diagnostic accuracy (n = 20), missing specification of or improper reference standards (n = 16, i.e. follow‐up ultrasound examination, diagnostic peritoneal lavage (DPL), or clinical observation), or penetrating injuries (n = 13). Reasons for exclusions are summarised in Figure 1.
Methodological quality of included studies
We evaluated the methodological quality of individual studies using the QUADAS‐2 tool and summarised quality assessments per fulfilled QUADAS‐2 domain (Figure 2; Figure 3). Poor reporting, especially in the patient selection and reference standard domains, hampered conclusive judgements about the risk of bias. Only five studies had a low risk of bias in all four critical domains (Benya 2000; Coley 2000; Emery 2001; Soudack 2004; Verbeek 2014). We rated at least two risk‐of‐bias domains as unclear or high in 19 studies.

Risk of bias and applicability concerns summary: review authors' judgements about each domain for each included study
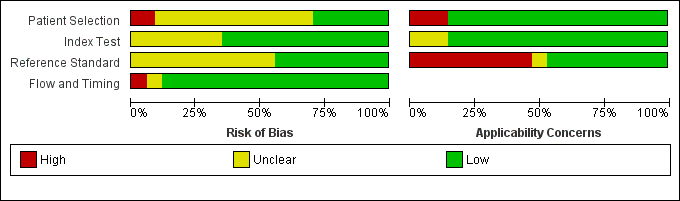
Risk of bias and applicability concerns graph: review authors' judgements about each domain presented as percentages across included studies
Patient selection
Three studies had a high risk of bias with regard to patient selection due to non‐consecutive enrolment of participants (e.g. inconsistent availability of designated sonographers, refusal of informed consent) and inappropriate exclusions (e.g. exclusion of patients with underlying diseases associated with intra‐abdominal fluid) (Ojaghi 2014; Talari 2015; Zhou 2012). Eleven studies had an unclear risk of bias due to non‐consecutive enrolment of patients (Becker 2010; Blaivas 2005; Cheung 2012; Clevert 2008; Corbett 2000; Fox 2011; Hsu 2007; Kendall 2009; Smith 2010; Valentino 2010; Wong 2014). We rated the patient inclusion procedure as unclear for 10 studies (Calder 2017; Catalano 2009; Dolich 2001; Friese 2007; Iqbal 2014; Kärk 2012; McKenney 1994; Nandipati 2011; Todd Miller 2003; Zhang 2006).
Index test
Unclear risk of bias ratings in both index test and reference standard domains originated mainly from missing or unclear information about hardware standards (e.g. machine specifications missing, no information on the number of imaging planes, etc.) or the qualification of operators, or both. Reported qualifications of POCS examiners ranged from attendance of an eight‐hour ultrasound course in Hsu 2007 to 10 years of experience in Menichini 2015. We rated eight studies as at unclear risk of bias due to a lack of information regarding the skills of sonographers and insufficient specification about whether index test results were interpreted without knowledge of other imaging test results (Calder 2017; Hsu 2007; Kärk 2012; Kendall 2009; McElveen 1997; McKenney 1994; Wong 2014; Zhou 2012).
Reference standard
We rated 12 studies as having an unclear risk of bias due to missing technical specifications for the reference imaging test (Calder 2017; Cheung 2012; Dolich 2001; Iqbal 2014; Kärk 2012; Kumar 2015; McElveen 1997; Nandipati 2011; Smith 2010; Tso 1992; Wong 2014; Zhou 2012). Information concerning the diagnostic reference standard was generally far scarcer than details about the index test.
Flow and timing
Most studies had a low risk of bias with regard to the examination flow and timing domain. Two studies employed diagnostic reference standards conditional on the result of ultrasound exams in some, McElveen 1997, or all, Menichini 2015, of the examined participants.
Findings
Diagnostic performance of individual studies comparing POCS with reference standard
Coupled forest plots of individual studies' sensitivities and specificities along with true positives (TP), false positives (FP), false negatives (FN), and true negatives (TN) are depicted in Figure 4. The sensitivity of POCS ranged from 0.26 (95% CI 0.14 to 0.42) to 1.00 (95% CI 0.74 to 1.00). Specificity ranged from 0.59 (95% CI 0.44 to 0.73) to 1.00 (95% CI 0.97 to 1.00). A graphical interpretation of coupled forest plots of individual studies' sensitivities and specificities did not indicate any threshold effect, therefore we considered the bivariate model to be the appropriate pooling procedure.
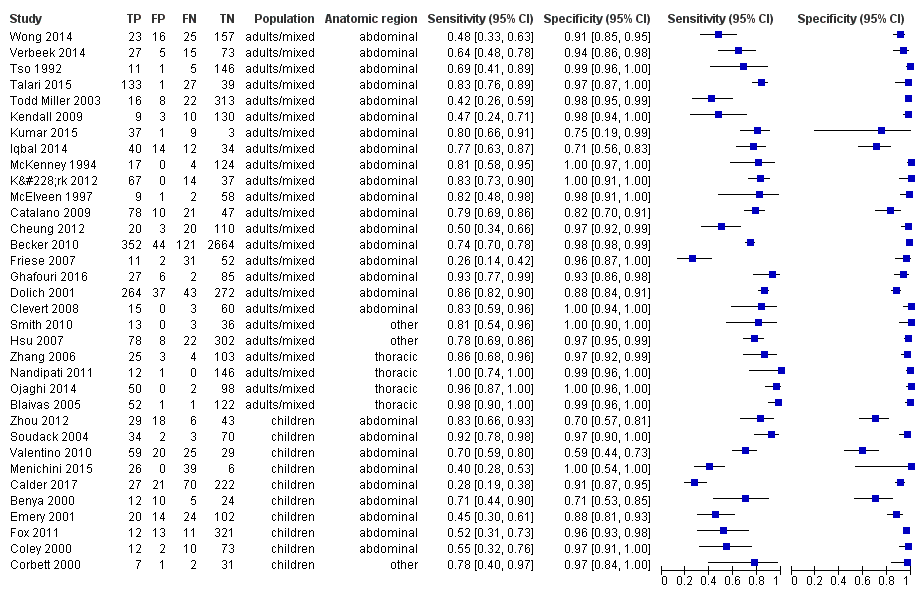
Coupled forest plots of sensitivity and specificity. TP = true positive; FP = false positive; FN = false negative; TN = true negative
Estimates derived from the bivariate model comparing POCS with reference standard
Figure 5 shows the pooled summary point for sensitivity and specificity derived from the bivariate model with corresponding 95% confidence and prediction regions. Summary estimates of sensitivity and specificity were 0.74 (95% CI 0.65 to 0.81) and 0.96 (95% CI 0.94 to 0.98). Corresponding positive and negative LRs were 18.5 (95% CI 10.8 to 40.5) and 0.27 (95% CI 0.19 to 0.37); PPV was 0.88 (95% CI 0.81 to 0.94); and NPV was 0.90 (95% CI 0.87 to 0.93). The observed median prevalence of blunt thoracoabdominal trauma in the total cohort was 28%. In a virtual population of 1000 patients, assuming the median prevalence of 28%, POCS would miss 73 patients with injuries, and falsely suggest the presence of injuries in another 29 patients.
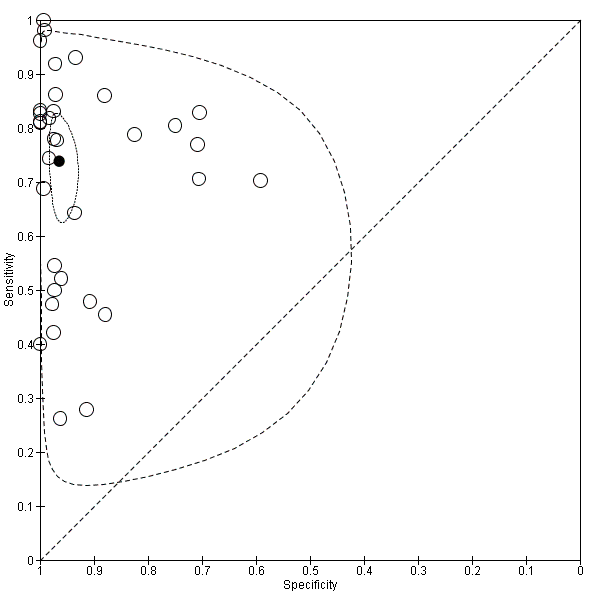
Summary receiver operating characteristic (ROC) plot of sensitivity and specificity of all 34 included studies. The solid circle represents the summary estimate of sensitivity and specificity. The summary estimate is surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.
Heterogeneity
The prediction region around the summary estimate in Figure 5 indicates with 95% confidence where the true sensitivity and specificity of POCS would be expected in a future study. As indicated by the width of the region, there was considerable heterogeneity between studies. Regarding sensitivity, the 95% prediction region varied from 0.14 to 0.98, while the specificity of future studies was estimated to range from 0.42 to 1.00. This marked between‐study heterogeneity needs further exploration.
a. Effect of reference standard
Each individual study used CT as confirmative imaging modality, either as a single gold standard or in combination with other reference tests. In 25 studies, target conditions were confirmed exclusively with CT, and in seven studies with CT and laparotomy. There was no difference in POCS sensitivity and specificity when compared with CT or CT plus laparotomy (Chi2 = 0.18; P value (overall effect) = 0.9160; CT: 0.75 (95% CI 0.63 to 0.84) and 0.97 (95% CI 0.93 to 0.98), CT plus laparotomy: 0.73 (95% CI 0.58 to 0.84) and 0.95 (95% CI 0.87 to 0.98)).
b. Effect of target condition
Twenty‐two studies assessed the diagnostic accuracy of POCS targeting surrogate measures like free fluid (18 studies) or air (four studies). Three studies aimed to assess solid organ damage, and another seven studies targeted both free fluid and direct signs of organ injuries. The individual target condition mainly affected specificity estimates (Chi2 = 9.10; P value (overall effect) = 0.0106). Sensitivity of POCS limited to detecting free fluid/air was 0.78 (95% CI 0.68 to 0.85), compared to 0.80 (95% CI 0.73 to 0.85) for complete assessment (Chi2 = 0.06; P value (pair‐wise) = 0.8100). Related specificities were 0.97 (95% CI 0.96 to 0.99) and 0.88 (95% CI 0.70 to 0.96), respectively (Chi2 = 8.08; P value (pair‐wise) = 0.0045). Coupled forest plots for limited assessment (Figure 6) and complete assessment (Figure 7) show greater variation in specificity in studies targeting both free fluid and direct signs of organ injuries compared to studies aimed only at free fluid or free air.
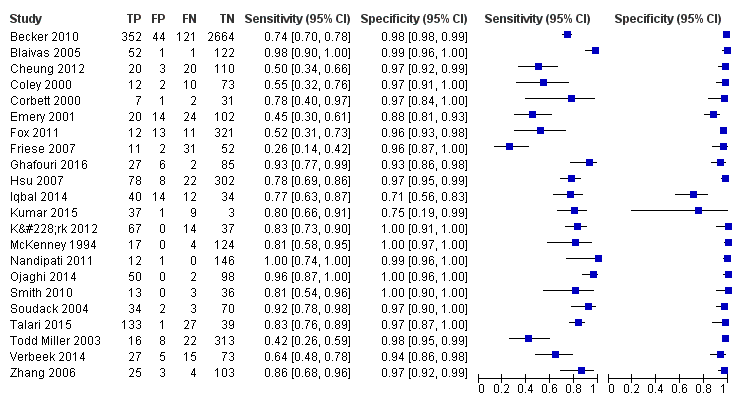
Coupled forest plots of sensitivity and specificity for studies targeting only free fluid or free air (n = 22). TP = true positive; FP = false positive; FN = false negative; TN = true negative
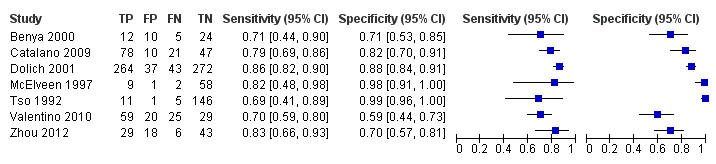
Coupled forest plots of sensitivity and specificity for studies considering both surrogates and organ lacerations (n = 7). TP = true positive; FP = false positive; FN = false negative; TN = true negative
c. Effect of participant age
Ten studies included only children under 18 years of age, whereas 24 studies involved adults or a largely adult population. Participant age was associated with significantly different estimates of both sensitivity and specificity (Chi2 = 7.32; P value (overall effect) = 0.0258). Pooled sensitivity of POCS was 0.63 (95% CI 0.46 to 0.77) in children and 0.78 (95% CI 0.69 to 0.84) in an adult or mixed population (Chi2= 54.91; P value (pair‐wise) < 0.0001). Associated specificities were 0.91 (95% CI 0.81 to 0.96) and 0.97 (95% CI 0.96 to 0.99) (Chi2 = 19.88; P value (pair‐wise) < 0.0001). Figure 8 depicts individual sensitivity and specificity estimates along with summary points, 95% confidence regions, and 95% prediction regions for both paediatric and non‐paediatric studies. Trials including only children are depicted by means of black dots, while trials with a predominantly adult population are shown as red dots. Figure 4 illustrates sensitivities and specificities from individual studies for non‐paediatric (first 24 studies) and paediatric populations (last 10 studies).
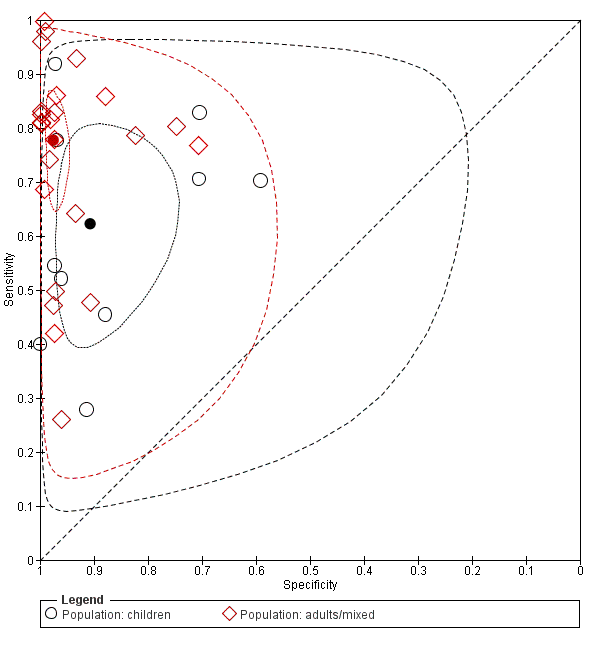
Summary receiver operating characteristic (ROC) plot of sensitivity and specificity: paediatric studies (n = 10; indicated in black) versus non‐paediatric studies (n = 24; indicated in red). The solid circles represent the summary estimates of sensitivity and specificity. The summary estimates are surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.
d. Effect of type of injury
Twenty‐seven studies targeted abdominal injuries; four studies addressed thoracic trauma; two studies addressed both; and one study examined blunt truncal trauma without further specification. We tested the influence of the anatomic region on the basic model by adding a binary covariate that dichotomised the injury type into thoracic or abdominal trauma. Based on 31 studies, this led to significantly different estimates of sensitivity and specificity (Chi2 = 17.36; P value (overall effect) = 0.0002). Sensitivity of POCS for abdominal and thoracic trauma was 0.68 (95% CI 0.59 to 0.75) and 0.96 (95% CI 0.88 to 0.99), respectively (Chi2 = 13.22; P value (pair‐wise) = 0.0003). Specificity was 0.95 (95% CI 0.92 to 0.97) and 0.99 (95% CI 0.97 to 1.00), respectively (Chi2 = 5.39; P value (pair‐wise) = 0.0202). Individual sensitivities and specificities for abdominal trauma, thoracic trauma, and trauma that is not exclusively abdominal or thoracic (i.e. both abdominal and thoracic trauma, truncal trauma) are displayed in Figure 4. Individual and average estimates of sensitivity and specificity, and both 95% confidence regions and 95% prediction regions around the summary estimates for thoracic and abdominal studies separately are illustrated in Figure 9. For abdominal trauma, the accuracy values are widely scattered across studies, whereas sensitivity and specificity values are consistently high when targeting only thoracic trauma.
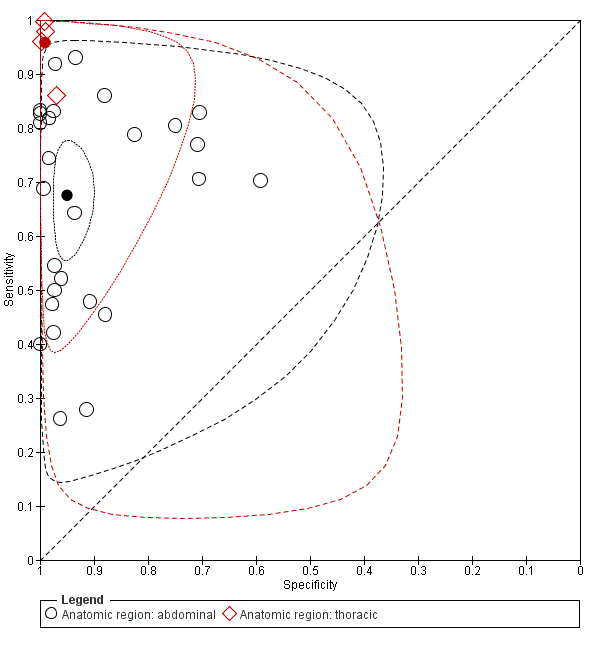
Summary receiver operating characteristic (ROC) plot of sensitivity and specificity: abdominal studies (n = 27; indicated in black) versus thoracic studies (n = 4; indicated in red). The solid circles represent the summary estimates of sensitivity and specificity. The summary estimates are surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.
Sensitivity analysis
a. Effect of study quality
We performed sensitivity analyses to investigate the effect of study quality on diagnostic accuracy estimates separately for each of the QUADAS‐2 key domains. Study quality did not have a substantial effect on either sensitivity or specificity estimates in any of the four domains. Sensitivity and specificity estimates for studies with low risk of bias were as follows: patient selection (9 studies) 0.75 (95% CI 0.63 to 0.85) and 0.93 (95% CI 0.83 to 0.98), index test (22 studies) 0.77 (95% CI 0.66 to 0.85) and 0.97 (95% CI 0.94 to 0.98), reference standard (11 studies) 0.77 (95% CI 0.60 to 0.89) and 0.97 (95% CI 0.93 to 0.99), flow and timing (30 studies) 0.74 (95% CI 0.65 to 0.81) and 0.96 (95% CI 0.93 to 0.98).
b. Effect of two independent reviewers within original studies
In two original studies (Benya 2000; Ghafouri 2016), sonograms and CT examinations were evaluated independently by two trialists, resulting in two different accuracy values for each reviewer. In order to analyse the influence of reviewers' decision on pooled accuracy estimates, we added both reviewers' lower accuracy estimates (Main analysis set) to one set and both reviewers' higher accuracy estimates to another set (Sensitivity analysis set) and assessed the differences; we detected no difference in either diagnostic accuracy estimate. The summary estimates of sensitivity and specificity along with CIs were identical in both sets with sensitivity estimates of 0.74 (95% CI 0.65 to 0.81) and specificity estimates of 0.96 (95% CI 0.94 to 0.98). The positive and negative LRs differed marginally with 20.9 (95% CI 12.0 to 36.5) and 0.27 (95% CI 0.20 to 0.37) in the Main analysis set compared with 20.8 (95% CI 11.8 to 36.8) and 0.27 (95% CI 0.20 to 0.37) in the Sensitivity analysis set.
c. Effect of patient age
When including only studies with patients under 18 years of age, sensitivity and specificity values were lower than in the analysis that included adults. In the 10 paediatric studies with 1384 participants, sensitivity was estimated at 0.62 (95% CI 0.47 to 0.75) and specificity at 0.91 (95% CI 0.81 to 0.96) (see summary of findings Table 1). Positive LR with 6.9 (95% CI 2.5 to 18.8), PPV with 0.76 (95% CI 0.53 to 0.89), and NPV with 0.84 (95% CI 0.77 to 0.90) were lower, and negative LR was higher with 0.42 (95% CI 0.26 to 0.65) than in the complete set of studies. In a virtual cohort of 1000 children having sustained blunt trauma, thoracoabdominal injuries would be missed in 118 cases (compared to 73 in the overall cohort), and 62 children would be falsely diagnosed as having sustained injuries (compared to 29 in the overall cohort).
Discusión
Resumen de los resultados principales
(ver Resumen de los hallazgos tabla 1)
En esta revisión sistemática se incluyeron 34 estudios (con 8635 participantes) que evaluaron la exactitud diagnóstica de la ecografía a pie de cama (EPC) para diagnosticar lesiones toracoabdominales en pacientes con traumatismo cerrado. Las estimaciones resumidas de la sensibilidad y la especificidad fueron 0,74 (intervalo de confianza [IC] del 95%: 0,65 a 0,81) y 0,96 (IC del 95%: 0,94 a 0,98). Las razones de verosimilitud negativa y positiva correspondientes fueron 18,5 (IC del 95%: 10,8 a 40,5) y 0,27 (IC del 95%: 0,19 a 0,37), respectivamente. No hubo un efecto umbral. El riesgo de sesgo se valoró en gran parte como incierto debido a la información insuficiente, en especial en cuanto a los dominios de la selección de los pacientes y el estándar de referencia.
Hubo heterogeneidad significativa en cuanto a la sensibilidad y la especificidad entre los estudios, que fue explicada en parte por las edades de los pacientes, el tipo de lesión y la afección objetivo. En los niños, la sensibilidad agrupada de la EPC fue 0,63 (IC del 95%: 0,46 a 0,77), en comparación con 0,78 (IC del 95%: 0,69 a 0,84) en una población adulta o mixta. La especificidad asociada fue 0,91 (IC del 95%: 0,81 a 0,96) y 0,97 (IC del 95%: 0,96 a 0,99). Las comparaciones pareadas para la sensibilidad y para la especificidad produjeron valores de p menores de 0,0001. Si se considera el número bastante grande de estudios en ambos grupos (es decir, diez estudios pediátricos versus 24 estudios no pediátricos), lo anterior indica una diferencia real entre ambos grupos que no se puede explicar por el azar u otras características. Para el traumatismo abdominal, la EPC tuvo una sensibilidad de 0,68 (IC del 95%: 0,59 a 0,75) y una especificidad de 0,95 (IC del 95%: 0,92 a 0,97). Para las lesiones de tórax, la sensibilidad y la especificidad fueron 0,96% (IC del 95%: 0,88% a 0,99%) y 0,99% (IC del 95%: 0,97% a 1,00%), respectivamente. Sin embargo, solo cuatro estudios tuvieron como objetivo exclusivamente las lesiones torácicas y ninguno reclutó niños, en los que los cálculos de la exactitud parecen ser en general inferiores. La afección objetivo individual afectó principalmente los cálculos de la especificidad, con una especificidad de 0,97 (IC del 95%: 0,96 a 0,99) para las evaluaciones limitadas al líquido/aire libre y una especificidad de 0,88 (IC del 95%: 0,70 a 0,96) para las evaluaciones completas que también incluyeron signos directos de daño de órganos.
Los cálculos resumidos de la sensibilidad y la especificidad se mantuvieron similares en los estudios con bajo riesgo de sesgo en los cuatro dominios (con una variación de 0,74 a 0,77 y 0,93 a 0,97; respectivamente). Cuando solo se incluyeron niños, los cálculos resumidos fueron inferiores en comparación con el análisis principal, con una sensibilidad de 0,62 (IC del 95%: 0,47 a 0,75) y una especificidad de 0,91 (IC del 95%: 0,81 a 0,96).
En una cohorte virtual de 1000 pacientes, si se supone una mediana de la prevalencia observada de traumatismo toracoabdominal del 28%, la EPC pasaría por alto a 73 pacientes con lesiones e indicaría falsamente la presencia de lesiones en otros 29 pacientes. En una cohorte de niños solamente, la EPC pasaría por alto a 118 pacientes con lesiones e indicaría falsamente la presencia de lesiones en otros 62 pacientes.
Fortalezas y limitaciones de la revisión
Se realizó una búsqueda bibliográfica exhaustiva en las principales bases de datos electrónicas utilizando una estrategia de recuperación reproducible. Con 2296 registros examinados y 34 estudios elegibles, existe certeza de que el conjunto de datos constituye, como mínimo, una muestra representativa y, en el mejor de los casos, una serie completa de estudios que investigan la exactitud diagnóstica de la EPC en pacientes con traumatismo cerrado. Se incluyeron filtros de exactitud de la prueba diagnóstica (EPD) en las estrategias de búsqueda en Ovid MEDLINE y Ovid Embase, como indicó el Especialista en Información del Grupo Cochrane de Lesiones, en concordancia con el protocolo. Los filtros de búsqueda metodológica se utilizan con frecuencia para reducir el gran número de estudios primarios y centrar la búsqueda en las citas más relevantes (Lefebvre 2017). Las recomendaciones actuales no apoyan el uso de filtros metodológicos, ya que pueden deteriorar la sensibilidad y la precisión (Beynon 2013). Aunque no se conoce que se haya pasado por alto algún estudio de exactitud importante con el algoritmo de búsqueda, el uso de un filtro de búsqueda metodológica podría representar una posible limitación de esta revisión.
El número relativamente grande de investigaciones permitió agrupar los cálculos resumidos de la sensibilidad y la especificidad y explorar las posibles fuentes de heterogeneidad. El uso de preguntas de señalización adaptadas y específicas de la revisión en la herramienta QUADAS‐2 permitió realizar una evaluación personalizada de la calidad metodológica de todos los estudios incluidos. Desafortunadamente, no fue posible la evaluación de la calidad metodológica debido a la importante falta de información en los estudios originales. Se investigó la influencia de la calidad deficiente de los estudios al realizar análisis de sensibilidad por separado para cada dominio de riesgo de sesgo, que mostró que la calidad de los estudios no influyó de manera importante en los cálculos de la exactitud diagnóstica.
Hubo heterogeneidad apreciable entre los estudios, visible por la región de predicción del 95% bastante amplia en la Figura 5. Como hay más pacientes con la afección objetivo en comparación con los que no la presentan, la región de predicción del 95% para la sensibilidad (0,14 a 0,98) fue mayor que la de la especificidad (0,42 a 1,00). Sin embargo, fue posible explicar en parte la heterogeneidad por las características de los estudios como la edad de los participantes, la afección objetivo y el tipo de lesión. Aún es polémico el rendimiento de la EPC en los niños (Holmes 2007). La menor especificidad observada en esta revisión se puede deber al número desproporcionadamente mayor de evaluaciones completas de las lesiones abdominales en los estudios en poblaciones pediátricas en comparación con los estudios en adultos.
La mayor sensibilidad y especificidad de la EPC en los estudios que solo examinan el tórax, en comparación con los estudios que se centran en el abdomen, coincide con revisiones anteriores (Alrajab 2013; Alrajhi 2012; Ding 2011; Ebrahimi 2014) En la presente revisión, la evaluación del líquido libre y de las lesiones de órganos por EPC dio lugar a una especificidad menor en comparación con la evaluación completa, lo que coincide con otros resultados publicados (p.ej., Poletti 2003).
Debido a información que faltaba no fue posible explorar algunas características (es decir, ambiente, pericia y antecedentes de los operadores, equipo, umbrales de la prueba) como fuentes de heterogeneidad. Solo dos estudios describieron el tratamiento de los resultados no concluyentes: en Iqbal 2014, los resultados no concluyentes se trataron como resultados positivos de la prueba, y en Dolich 2001, los resultados indeterminados se excluyeron de los cálculos de la sensibilidad y la especificidad, y el porcentaje de resultados indeterminados fue de solo el 1%. No se espera que el número generalmente bajo de resultados no concluyentes de la prueba en los estudios primarios afecte los resultados de la presente revisión. Fue necesario modificar la clasificación original de los estándares de referencia y la edad de los participantes para investigar la heterogeneidad. Como la tomografía computarizada (TC) se utilizó como prueba de referencia en todos los estudios, se comparó la exactitud diagnóstica de la EPC con la TC y con la TC más laparotomía. Debido al número pequeño de estudios que incluyeron exclusivamente adultos, se decidió comparar las cohortes de niños solo con los estudios que incluyeron poblaciones en edad adulta o mixtas. Se prefirió este enfoque al de dividir los datos en dos partes según la edad mediana o promedio de los participantes.
Los participantes se clasificaron como prueba positiva si se detectó cualquiera de las afecciones objetivo, independientemente del hecho de que las afecciones objetivo podían diferir entre la prueba índice y el estándar de referencia. En su mayoría, los estudios originales (es decir, 25 de 34) utilizaron afecciones objetivo similares para la prueba índice y el estándar de referencia, por lo que no hubo disparidad. Sin embargo, el informe no transparente en los otros estudios impidió correlacionar la fuente de hemorragia entre ambos procedimientos diagnósticos, lo que puede dar lugar a una disparidad con respecto a la afección objetivo. En este caso no se supone una disparidad apreciable; sin embargo, no es posible excluir un efecto sobre los cálculos de la exactitud de la prueba.
Los estándares de referencia apropiados se limitaron a las pruebas de imagen o invasivas predefinidas (es decir, TC, imagen por resonancia magnética [IRM], laparotomía, laparoscopia, toracotomía, toracoscopia, autopsia), lo que garantizó la estimación exacta de las sensibilidades y las especificidades de la EPC como prueba índice. Sin embargo, no fue posible detectar investigaciones que utilizaran la IRM, la laparoscopia, la toracotomía o la toracoscopia como único estándar de referencia, como se especifica en los criterios de inclusión y exclusión, por lo que no fue posible evaluar la exactitud diagnóstica de la EPC comparada con estas técnicas de diagnóstico. Por lo tanto, la exactitud diagnóstica de la EPC se refiere principalmente a la TC como comparador, en lugar de otro estándar de referencia, lo que puede limitar la generalización de esta revisión.
Aplicabilidad de los hallazgos a la pregunta de la revisión
Para generar evidencia clínicamente realista y relevante, se mantuvieron los criterios de inclusión bastante amplios. En consecuencia, las características de los estudios individuales y los participantes variaron de manera significativa, por ejemplo, en cuanto a la edad, la región corporal afectada, las afecciones objetivo, la pericia de los operadores, las especificaciones del equipo, etc. Fue sorprendente encontrar que, aunque estas variaciones dieron lugar a heterogeneidad marcada en los cálculos de la sensibilidad y la especificidad de los estudios, también permitieron comparar los cálculos de la exactitud en diversos contextos y aplicaciones de la EPC.
Las inquietudes acerca de la aplicabilidad en la selección de los participantes, la prueba índice y los estándares de referencia se evaluaron al utilizar preguntas adaptadas en la herramienta QUADAS‐2. De los 34 estudios incluidos, 11 se asociaron con inquietudes bajas acerca de la aplicabilidad(Benya 2000; Blaivas 2005; Coley 2000; Emery 2001; Ghafouri 2016; Kendall 2009; Nandipati 2011; Ojaghi 2014; Talari 2015; Todd Miller 2003; Zhang 2006). En los dominios selección de los pacientes y prueba índice, 29 estudios mostraron inquietudes bajas acerca de la aplicabilidad. En la selección de los pacientes, se les asignaron inquietudes altas a cinco estudios debido a criterios de inclusión limitados (es decir, solo fracturas pelvianas (Friese 2007; Verbeek 2014); solo traumatismo leve, Menichini 2015, o solo traumatismo grave,Corbett 2000; o con lesiones limitadas de órganos solo (Kärk 2012)). Se consideró que cinco estudios tuvieron calificaciones poco claras en el dominio de la prueba índice debido a la información que faltaba acerca de las áreas corporales examinadas (Calder 2017; Clevert 2008; Valentino 2010; Wong 2014; Zhou 2012). El uso condicional de los estándares de referencia según los resultados de la observación clínica, el examen por ecografía o la estabilidad hemodinámica de los participantes dio lugar a 16 inquietudes altas en la calificación de la aplicabilidad en el dominio del estándar de referencia.
En resumen, el 85% de todos los estudios incluidos se calificó como de preocupación baja para la aplicabilidad en los dominios de selección de los pacientes y prueba índice, mientras que solo el 47% de los estudios se calificó como de preocupación baja en los dominios del estándar de referencia. Aunque el espectro de participantes incluidos en esta revisión puede reflejar de manera apropiada la población objetivo, y las pruebas índice utilizadas en los estudios incluidos pueden no diferir considerablemente de las de la práctica clínica, el espectro de estándares de referencia puede no corresponder en su totalidad con la amplia variedad de pruebas que en realidad se utilizan en el contexto del traumatismo toracoabdominal.

Study flow diagram for the search conducted on 15 July 2017.

Risk of bias and applicability concerns summary: review authors' judgements about each domain for each included study

Risk of bias and applicability concerns graph: review authors' judgements about each domain presented as percentages across included studies

Coupled forest plots of sensitivity and specificity. TP = true positive; FP = false positive; FN = false negative; TN = true negative

Summary receiver operating characteristic (ROC) plot of sensitivity and specificity of all 34 included studies. The solid circle represents the summary estimate of sensitivity and specificity. The summary estimate is surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.
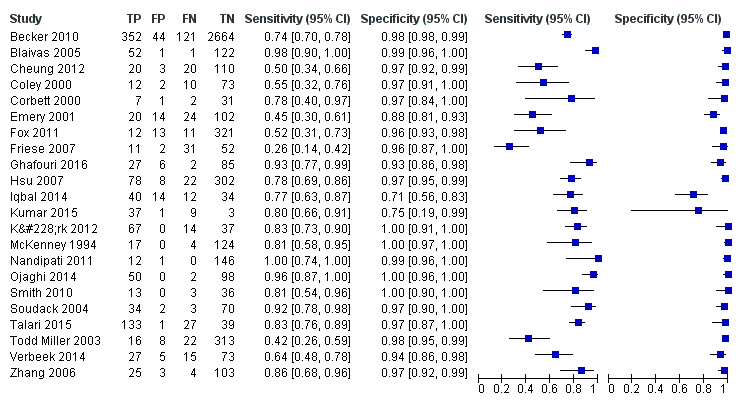
Coupled forest plots of sensitivity and specificity for studies targeting only free fluid or free air (n = 22). TP = true positive; FP = false positive; FN = false negative; TN = true negative

Coupled forest plots of sensitivity and specificity for studies considering both surrogates and organ lacerations (n = 7). TP = true positive; FP = false positive; FN = false negative; TN = true negative

Summary receiver operating characteristic (ROC) plot of sensitivity and specificity: paediatric studies (n = 10; indicated in black) versus non‐paediatric studies (n = 24; indicated in red). The solid circles represent the summary estimates of sensitivity and specificity. The summary estimates are surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.

Summary receiver operating characteristic (ROC) plot of sensitivity and specificity: abdominal studies (n = 27; indicated in black) versus thoracic studies (n = 4; indicated in red). The solid circles represent the summary estimates of sensitivity and specificity. The summary estimates are surrounded by a dotted line representing the 95% confidence region and a dashed lined representing the 95% prediction region.

Main analysis set.

Sensitivity analysis set with lower sensitivity/specificity values in two original studies.
| Population | Patients of any age and gender who sustained any type of blunt injury in a civilian scenario | |||||||
| Setting | Clinical evaluation at hospitals of any care level | |||||||
| Index test | Point‐of‐care sonography (POCS) as the primary imaging tool | |||||||
| Reference standard | Computed tomography (CT), magnetic resonance imaging (MRI), laparotomy, laparoscopy, thoracotomy, thoracoscopy, autopsy | |||||||
| Findings |
| |||||||
| Limitations |
| |||||||
| No. of participants (studies) | Summary sensitivity (95% CI) | Summary specificity (95% CI) | Summary LR+ (95% CI) | Summary LR‐ (95% CI) | Positive predictive value (95% CI) | Negative predictive value (95% CI) | Consequences in a virtual cohort of 1000a | |
| Missed injuries | Overtreated | |||||||
| 8635 (34) | 0.74 (0.65 to 0.81) | 0.96 (0.94 to 0.98) | 18.5 (10.8 to 40.5) | 0.27 (0.19 to 0.37) | 0.88 (0.81 to 0.94) | 0.90 (0.87 to 0.93) | 73 (If 280 people suffer an injury through trauma, 207 will be identified as injured, and 73 will be missed.) | 29 (If 720 people do not suffer an injury through trauma, 29 will be treated as though they had been injured, i.e. overtreated.) |
| Sensitivity analysis with a children‐only cohort | ||||||||
| 1384 (10) | 0.62 (0.47 to 0.75) | 0.91 (0.81 to 0.96) | 6.9 (2.5 to 18.8) | 0.42 (0.26 to 0.65) | 0.76 (0.53 to 0.89) | 0.84 (0.77 to 0.90) | 118 (If 310 children suffer an injury through trauma, 192 will be identified as injured, and 118 will be missed.) | 62 (If 690 children do not suffer an injury through trauma, 62 will be treated as though they had been injured, i.e. overtreated.) |
| aThe median prevalence was 28% for the complete study population and 31% for the children‐only cohort. | ||||||||
| Abbreviations CI: confidence interval | ||||||||
| Investigation of heterogeneity | Number of studies | Summary sensitivity (95% CI) | Summary specificity (95% CI) | Chi2a | P valueb |
| Reference standard | |||||
| Single CT | 25 | 0.75 (0.63 to 0.84) | 0.97 (0.93 to 0.98) | 0.18 (overall) | 0.9160 (overall) |
| CT plus laparotomy | 7 | 0.73 (0.58 to 0.84) | 0.95 (0.87 to 0.98) | ||
| Target condition | |||||
| Limited to free fluid/free air | 22 | 0.78 (0.68 to 0.85) | 0.97 (0.96 to 0.99) | 9.10 (overall) 0.06 (sensitivity) 8.08 (specificity) | 0.0106 (overall) 0.8100 (sensitivity) 0.0045 (specificity) |
| Free fluid/free air and organ injuries/vascular lesions | 7 | 0.80 (0.73 to 0.85) | 0.88 (0.70 to 0.96) | ||
| Age of participant | |||||
| Children | 10 | 0.63 (0.46 to 0.77) | 0.91 (0.81 to 0.96) | 7.32 (overall) 54.91 (sensitivity) 19.88 (specificity) | 0.0258 (overall) 0.0000 (sensitivity) 0.0000 (specificity) |
| Adults/mixed | 24 | 0.78 (0.69 to 0.84) | 0.97 (0.96 to 0.99) | ||
| Type of injury | |||||
| Abdominal injury | 27 | 0.68 (0.59 to 0.75) | 0.95 (0.92 to 0.97) | 17.36 (overall) 13.22 (sensitivity) 5.39 (specificity) | 0.0002 (overall) 0.0003 (sensitivity) 0.0202 (specificity) |
| Thoracic injury | 4 | 0.96 (0.88 to 0.99) | 0.99 (0.97 to 1.00) | ||
| aLarge values of the Chi2 statistic indicate that test performance may be associated with the particular covariate. bP values < 0.05 indicate statistical evidence that sensitivity and/or specificity differ between the examined groups. | |||||
| Abbreviations CI: confidence interval | |||||
| Test | No. of studies | No. of participants |
| 1 Main analysis set Show forest plot | 34 | 8635 |
| 2 Sensitivity analysis set with lower sensitivity/specificity values in two original studies Show forest plot | 34 | 8635 |

