Momento adecuado para la inhalación de solución salina hipertónica en la fibrosis quística
Resumen
Antecedentes
La inhalación de solución salina hipertónica mejora la reología del esputo, acelera la limpieza mucociliar y mejora los resultados clínicos de los pacientes con fibrosis quística.
Objetivos
Determinar si el momento adecuado de inhalación de solución salina hipertónica (con relación a las técnicas de limpieza de las vías respiratorias o al momento del día) tiene impacto sobre su eficacia clínica en los pacientes con fibrosis quística.
Métodos de búsqueda
Se identificaron los ensayos controlados aleatorios y cuasialeatorios relevantes de los Registros de Ensayos Cochrane de Fibrosis Quística (Cochrane Cystic Fibrosis Trials Register), la Physiotherapy Evidence Database (PEDro) y las actas de congresos internacionales de fibrosis quística.
Fecha de la búsqueda más reciente en el Registro de Ensayos de Fibrosis Quística del Grupo Cochrane de Fibrosis Quística y Trastornos Genéticos: 19 diciembre 2016.
Criterios de selección
Cualquier ensayo de solución salina hipertónica en pacientes con fibrosis quística donde el momento adecuado de la inhalación fue el elemento aleatorio en el protocolo del estudio con: inhalación hasta seis horas antes de las técnicas de limpieza de las vías respiratorias en comparación con la inhalación durante las técnicas de limpieza de las vías respiratorias en comparación con la inhalación hasta seis horas después de las técnicas de limpieza de las vías respiratorias; o inhalación matutina comparada con inhalación vespertina con cualquier definición proporcionada por el autor.
Obtención y análisis de los datos
Ambos autores de la revisión evaluaron de forma independiente los ensayos identificados mediante la búsqueda para su posible inclusión en la revisión.
Resultados principales
Las búsquedas identificaron 97 informes de ensayos que representaron 46 estudios, de los cuales dos estudios (proporcionando datos sobre 63 participantes) cumplieron con los criterios de inclusión. Los dos estudios usaron un diseño cruzado. Ambos estudios presentaron un riesgo bajo de todos los tipos de sesgo con la excepción de que no se realizó el cegamiento de los participantes ni de los terapeutas que aplicaron los tratamientos. Los períodos de intervención variaron de un tratamiento a tres tratamientos en un día. Los efectos de los diversos regímenes en la función pulmonar fueron no significativos. La satisfacción se consideró significativamente inferior en una escala de 100 mm cuando la solución salina hipertónica se inhaló después de las técnicas de limpieza de las vías respiratorias: diferencias de medias 20,38 mm (intervalo de confianza del 95%: 12,10 a 28,66) en comparación con antes de las técnicas de limpieza de las vías respiratorias y 14,80 mm (intervalo de confianza del 95%: 5,70 a 23,90) en comparación con durante las técnicas. La efectividad percibida mostró resultados significativos similares. Otros resultados no fueron afectados por el régimen del momento adecuado utilizado. Ningún ensayo comparó la inhalación de solución salina hipertónica matutina versus vespertina.
Conclusiones de los autores
A los pacientes con fibrosis quística se los puede alentar a que inhalen solución salina hipertónica antes o durante las técnicas de limpieza de las vías respiratorias para maximizar la eficacia y la satisfacción percibidas, aunque estos regímenes del momento adecuado pueden no tener un mejor efecto sobre la función pulmonar que la inhalación después de las técnicas de limpieza de las vías respiratorias. Como la eficacia a largo plazo de la solución salina hipertónica sólo está establecida para las inhalaciones dos veces al día, los médicos deben recomendar a los pacientes la inhalación de solución salina hipertónica con esta frecuencia. Sin embargo, si sólo se tolera una dosis por día, el momento del día en que se realiza la inhalación podría basarse en la comodidad o la tolerabilidad hasta que se disponga de más pruebas que comparen estos regímenes.
PICOs
Resumen en términos sencillos
Momento adecuado de inhalación de solución salina hipertónica en pacientes con fibrosis quística
Pregunta de la revisión
Se examinaron las pruebas acerca de si el momento adecuado (con relación a las técnicas de limpieza de las vías respiratorias o al momento del día) de la inhalación de solución salina hipertónica (una solución de alta concentración de soluto, salada y estéril) a través de un nebulizador mejora las propiedades físicas del esputo, estimula la tos, mejora los resultados clínicos (como la función pulmonar) y mejora el efecto percibido de las técnicas de limpieza de las vías respiratorias en los pacientes con fibrosis quística.
Antecedentes
La inhalación regular de solución salina hipertónica mejora los resultados clínicos en los pacientes con fibrosis quística. Existen dudas sobre si es mejor inhalar la solución salina hipertónica antes, durante o después de la limpieza de las vías respiratorias con técnicas físicas, o sobre si es mejor inhalarla a la mañana o la tarde noche. Se realizaron búsquedas de ensayos que comparaban estos diferentes regímenes del momento adecuado.
Fecha de la búsqueda
Las pruebas están actualizadas hasta: 19 diciembre 2016.
Características de los estudios
La revisión incluyó dos estudios con 63 pacientes con fibrosis quística de entre 18 y 64 años de edad. Los estudios consideraron el impacto del momento adecuado de la inhalación de solución salina hipertónica con relación a las técnicas de limpieza de las vías respiratorias. Los estudios informaron los resultados inmediatos después de la inhalación de solución salina hipertónica antes, durante o después de las técnicas físicas de limpieza de las vías respiratorias. Ambos estudios fueron cortos, e incluían sólo uno a tres tratamientos de cada régimen del momento adecuado.
Resultados clave
Aunque los resultados como la función pulmonar no mostraron diferencias entre los regímenes, los pacientes con fibrosis quística percibieron que la inhalación de solución salina hipertónica antes o durante las técnicas de limpieza de las vías respiratorias fue más efectiva y satisfactoria que la inhalación de solución salina hipertónica después de la limpieza de las vías respiratorias. No se encontraron estudios que compararan la inhalación matutina y vespertina. Como la eficacia a largo plazo de la solución salina hipertónica sólo está establecida para las inhalaciones dos veces al día, los médicos deben recomendar a los pacientes la inhalación de solución salina hipertónica con esta frecuencia. Sin embargo, si sólo se tolera una dosis por día, el momento del día en el que se realice la inhalación se podría basar en la comodidad o la tolerabilidad hasta que se disponga de más pruebas.
Calidad de la evidencia
En general, la calidad de las pruebas fue muy buena. Los únicos temas que quizás hayan afectado la calidad se relacionaron con el hecho de que no fue posible realizar el cegamiento de los participantes al tratamiento recibido. Sin embargo, como los estudios fueron a corto plazo y la mayoría de los resultados significativos se basaron en la eficacia percibida, se necesitan estudios adicionales sobre el momento adecuado de la administración de la solución salina hipertónica.
Conclusiones de los autores
Antecedentes
Descripción de la afección
La fibrosis quística (FQ) es la enfermedad autosómica recesiva limitante para la vida más frecuente en personas de origen caucásico (Cutting 2002). La limpieza mucociliar presenta un deterioro en la FQ (Robinson 1996; Robinson 1997). La enfermedad pulmonar relacionada con la fibrosis quística es la causa principal de morbilidad y mortalidad (Buzzetti 2009).
Descripción de la intervención
La solución salina hipertónica es una solución estéril de agua salada administrada como un tratamiento nebulizado, generalmente a una concentración de entre un 3% y un 10% (composición por masa). Tradicionalmente, se nebulizan volúmenes de 3 ml a 10 ml (Elkins 2006c; Wark 2009). Se recomienda su uso a largo plazo (Button 2016).
Cada dosis de solución salina hipertónica por lo general se nebuliza inmediatamente antes de la limpieza de las vías respiratorias, aunque a veces se usan otros regímenes del momento adecuado en la práctica clínica. El efecto clínico de la solución salina hipertónica podría ser afectado por el momento adecuado de la administración con relación a las técnicas físicas de limpieza de las vías respiratorias (antes, durante o después) o con relación al momento del día (mañana o tarde noche).
De qué manera podría funcionar la intervención
Se ha demostrado que la solución salina hipertónica acelera la limpieza mucociliar en las vías respiratorias de los pacientes con FQ (Robinson 1996; Robinson 1997). Se cree que tres mecanismos contribuyen a esta mejoría en la limpieza mucociliar. El primero es la restauración del volumen eliminado de líquido superficial de la vía respiratoria, que llega al máximo casi inmediatamente después de una dosis, pero el cual puede mantenerse durante varias horas (Donaldson 2006). Los otros mecanismos son: la mejoría en la reología del moco (King 1997; Wills 1997), y la estimulación de la tos (Robinson 1996; Robinson 1997). El efecto general sobre la limpieza del moco probablemente es responsable de las mejorías clínicas significativas incluida la función pulmonar, la calidad de vida y la facilidad de la expectoración con el uso regular del tratamiento (Elkins 2006b; Eng 1996). Una revisión Cochrane de la solución salina hipertónica nebulizada para la FQ concluyó que se demostraron mejorías en el volumen espiratorio forzado en un segundo (VEF1) después de dos a cuatro semanas de tratamiento, y que mejoró la calidad de vida y las tasas de exacerbación pulmonar en comparación con las intervenciones de placebo después de 48 semanas de tratamiento (Wark 2009).
En los estudios controlados que establecían la eficacia de la solución salina hipertónica (Elkins 2006c; Eng 1996; Robinson 1996; Robinson 1997), cada dosis se nebulizó inmediatamente antes de la administración de las técnicas de limpieza de las vías respiratorias. Sin embargo, otros regímenes del momento adecuado pueden tener ventajas. La nebulización de solución salina hipertónica durante las técnicas de limpieza de las vías respiratorias podría ahorrar tiempo. También puede aprovechar el punto máximo inmediato en el volumen de líquido superficial de las vías respiratorias. La nebulización después de las técnicas de limpieza de las vías respiratorias puede aprovechar la reducción en la obstrucción de las vías respiratorias causada por el moco y así permitir la administración de solución salina hipertónica a una mayor porción del árbol bronquial.
En los ensayos clínicos que establecieron la eficacia del uso regular de solución salina hipertónica (Donaldson 2006; Elkins 2006c; Eng 1996), se usaron al menos dos dosis por día. Sin embargo, algunos individuos pueden tolerar (o por otras razones elegir) sólo una dosis por día. Para estos pacientes, la nebulización de la dosis en un momento particular del día puede afectar su eficacia. Debido a que la limpieza mucociliar espontánea es más rápida en las horas de vigilia que durante el sueño (Bateman 1978), la inhalación matutina de solución salina hipertónica puede aprovechar la limpieza mucociliar diurna más rápida y los efectos de desobstrucción de las actividades diurnas como el ejercicio (Wolff 1977). Algunos pacientes con FQ encuentran la inhalación vespertina más conveniente o informan que mejora la facilidad de la expectoración la mañana siguiente. Debido a que la limpieza mucociliar y la tos se suprimen durante la noche, la inhalación vespertina de solución salina hipertónica puede aumentar el tiempo de permanencia en las vías respiratorias, lo que quizás aumente su eficacia clínica.
Por qué es importante realizar esta revisión
A pesar de las fundamentaciones teóricas presentadas para justificar la investigación de los regímenes alternativos del momento adecuado en la sección anterior, también es posible que puedan tener efectos adversos sobre la eficacia, la tolerabilidad y la comodidad del tratamiento y sobre la duración de la sesión de limpieza de las vías respiratorias. Por ejemplo, la nebulización de solución salina hipertónica durante las técnicas de limpieza de las vías respiratorias podría aumentar la complejidad de la sesión general de limpieza de las vías respiratorias, y quizás se requeriría una modificación del equipo. La nebulización después de las técnicas de limpieza de las vías respiratorias posiblemente administre la solución salina hipertónica de una forma más directa al epitelio expuesto de la vía respiratoria, en lugar de a una capa de moco suprayacente, lo cual puede reducir la tolerabilidad. La administración vespertina puede aumentar la tos nocturna y los trastornos del sueño. Por lo tanto, es importante examinar la investigación bien diseñada que compara los regímenes.
Hay una carga alta de tratamiento asociada con la FQ tanto para las personas con la enfermedad como para los profesionales de atención. La inhalación de solución salina hipertónica se agrega a la duración del régimen general de tratamiento. Por lo tanto, aunque los diversos regímenes del momento adecuado presentan una eficacia clínica igual, es importante que la revisión también investigue si las intervenciones difieren en sus efectos sobre la duración de la sesión general de limpieza de las vías respiratorias, en su comodidad y en sus efectos secundarios.
Objetivos
Determinar si el momento adecuado de la inhalación de solución salina hipertónica, con relación a las técnicas físicas de limpieza de las vías respiratorias o al momento del día, tiene una repercusión sobre las medidas objetivas y subjetivas de la eficacia y la tolerabilidad clínica en los pacientes con FQ.
Métodos
Criterios de inclusión de estudios para esta revisión
Tipos de estudios
Ensayos aleatorios (publicados y no publicados). Se incluyeron ensayos con asignación aleatoria y asignación cuasialeatoria (p.ej. cuando la asignación a los grupos fue por alternancia). Los ensayos paralelos y cruzados reunieron los requisitos.
Tipos de participantes
Pacientes de cualquier edad y sexo con FQ diagnosticada por pruebas genéticas o pruebas de cloruro en el sudor o de diferencia de potencial nasal, incluidos todos los grados de gravedad de la enfermedad.
Tipos de intervenciones
Solución salina hipertónica nebulizada, cuando el momento adecuado de la inhalación era el elemento aleatorio en el protocolo de estudio:
-
inhalación de solución salina hipertónica hasta seis horas antes de aplicar las técnicas de desobstrucción de las vías respiratorias en comparación con la inhalación durante las técnicas de desobstrucción de las vías respiratorias;
-
inhalación de solución salina hipertónica hasta seis horas antes de aplicar las técnicas de desobstrucción de las vías respiratorias en comparación con la inhalación hasta seis horas después de aplicar las técnicas de desobstrucción de las vías respiratorias;
-
inhalación de solución salina hipertónica durante las técnicas de desobstrucción de las vías respiratorias, en comparación con hasta seis horas después de aplicar las técnicas de desobstrucción de las vías respiratorias;
-
inhalación matutina comparada con inhalación vespertina con cualquier definición proporcionada por el autor. Si no se definió, se aceptó desde la medianoche hasta el mediodía como inhalación matutina y desde el mediodía hasta la medianoche como vespertina.
Nota: muchos individuos realizan dos tratamientos con técnicas físicas de limpieza de las vías respiratorias por día. Incluso si estos tratamientos se realizan lo más alejado posible entre sí (es decir cada 12 horas), cualquier umbral mayor que seis horas significaría que la solución salina hipertónica denominada “antes” en realidad sería más cercana a “después” del tratamiento anterior con técnicas físicas de limpieza de las vías respiratorias. Por lo tanto, seis horas es el umbral más amplio posible para captar todos los ensayos potencialmente relevantes. Sin embargo, algunos de los mecanismos por los cuales el momento adecuado puede afectar el resultado son de corta duración. Por lo tanto, se realiza un análisis de sensibilidad que sólo considera los ensayos en los que la solución salina hipertónica se utiliza en el plazo de los 30 min de las técnicas (ver Análisis de sensibilidad).
El régimen del momento adecuado podía ser un tratamiento único o mantenerse en cualquier duración.
El tratamiento con solución salina hipertónica debía incluir como mínimo una dosis única con una concentración de al menos un 3%. Cuando los estudios mencionaban cointervenciones (como broncodilatadores y otros fármacos inhalados), se permitió la administración de los mismos siempre que fueran iguales en todos los días del ensayo y se administraran o antes o después del período durante el cual se utilizaba la solución salina hipertónica y las técnicas de limpieza de las vías respiratorias.
Las técnicas de desobstrucción de las vías respiratorias (TDVR) debían tener una duración mínima de diez minutos e incluir al menos uno de los siguientes:
-
Drenaje postural con percusión y vibración (DPPV). En otras revisiones esto se ha descrito como fisioterapia torácica convencional (FTC) (Elkins 2006c; Main 2009; van der Schans 2009);
-
ciclo activo de técnicas respiratorias (CATR): comprende la relajación o el control respiratorio, la técnica de espiración forzada (TEF), los ejercicios de expansión torácica y puede incluir drenaje postural o percusión (Robinson 2010);
-
drenaje autógeno (DA). Esta técnica respiratoria utiliza velocidades altas del flujo espiratorio en volúmenes pulmonares variables para mejorar la eliminación del mucus, mientras se evita el cierre de las vías respiratorias;
-
presión espiratoria positiva (PEP) (Elkins 2006a);
-
dispositivos oscilatorios orales que proporcionan PEP oscilatoria (como Flutter, Cornet y Acapella) o ventilación percusiva intrapulmonar, que proporciona oscilación continua de la presión del aire en las vías respiratorias a través de la boca (Morrison 2009);
-
dispositivos de oscilación torácica aplicados a través de un chaleco para proporcionar una oscilación externa de la pared torácica (Morrison 2009);
-
el ejercicio prescrito para la desobstrucción de las vías respiratorias, ya sea de forma independiente o como un complemento de otras técnicas.
Tipos de medida de resultado
Resultados primarios
-
Función pulmonar, es decir, cambio en la función pulmonar (medido en litros o % previsto). Si los valores de cambio no están disponibles, se usarán los valores finales posteriores al tratamiento. Se analizan por separado los valores en litros y como porcentaje teórico.
-
volumen espiratorio forzado en un segundo (VEF1)
-
capacidad vital forzada (CVF)
-
-
Resultados informados por el paciente, mediante escalas validadas o medidas de informe subjetivas
-
medidas de calidad de vida (CdV)
-
puntuaciones de los síntomas (incluida la tos, la tolerabilidad, el alivio subjetivo de la desobstrucción o la satisfacción con el tratamiento)
-
Resultados secundarios
-
Medidas de depuración del esputo, incluidas las medidas de limpieza mucociliar (evaluado de acuerdo a la depuración de los trazadores radiactivos) y las medidas objetivas del volumen de esputo
-
Medidas de la capacidad de ejercicio (máximo o submáximo medido de forma directa, o con una prueba de campo estándar)
-
Mortalidad (por todas las causas o relacionada con la FQ, analizadas por separado)
-
Otros parámetros pulmonares
-
flujo espiratorio forzado entre el 25% y el 75% de la capacidad vital (FEF25‐75)
-
)flujo forzado instantáneo máximo cuando queda un 25% de la CVF para espirar (FEM25))
-
capacidad pulmonar total (CPT)
-
volumen residual (VR)
-
capacidad funcional residual (CFR)
-
Índice de depuración de los pulmones (IDP)
-
-
Frecuencia de las exacerbaciones de infección respiratoria donde se describa una definición clara que demuestre un aumento de los síntomas o una disminución de la función pulmonar)
-
tasas de ingreso al hospital (definidas como el número de ingresos hospitalarios o días de hospitalización)
-
ciclos de antibióticos intravenosos (recibidos en el hospital o en el domicilio)
-
tratamientos ambulatorios (consultas en el hospital, visitas no programadas al médico)
-
-
Adherencia a los tratamientos inhalados, las técnicas de desobstrucción de las vías respiratorias y otros tratamientos
-
Efectos adversos como broncoespasmos, tos y disminución aguda de la función pulmonar.
Results
Description of studies
Results of the search
The searches identified 97 trial reports which represented 46 studies.
Included studies
Two trials were eligible for inclusion, which provided data for a total of 63 participants (Dentice 2012; Van Ginderdeuren 2011) (Figure 1). One trial has not yet been published in full but has been presented as an oral presentation at a conference (Van Ginderdeuren 2011). No trial was identified regarding timing of hypertonic saline inhalation in relation to time of day.
Trial characteristics
The two included studies were randomised, cross‐over trials with concealed allocation, intention to treat analysis and blinded assessors (Dentice 2012; Van Ginderdeuren 2011). They investigated the impact of timing of hypertonic saline inhalation in relation to airway clearance techniques. The inhalation blocks were for one day. In one trial, three treatments of the allocated timing regimen were performed on each of the three trial days (Dentice 2012). In the second trial, a single treatment of 30 minutes was undertaken on each of the three trial days (Van Ginderdeuren 2011). One day was solely autogenic drainage and did not include hypertonic saline inhalation. This arm of the trial was not relevant to the study question of this review so the data were not included.
Participants
Clarification of participant data was requested from the authors of the two studies. One trial included 50 adults (mean (SD) age 31 (10) years, range 18 to 64 years) with a confirmed diagnosis of cystic fibrosis who were clinically stable with an FEV₁ within 10% of the best recorded value in the last six months (Dentice 2012). This trial excluded people who were: hypertonic saline naïve or previously intolerant; lung transplant recipients; colonised with Burkholderia cepacia complex; not clinically stable; experienced haemoptysis greater than 60 mL within the last month or thrombocytopenia or pregnancy. The second trial recruited 13 hospitalised participants who were over 14 years (mean age 27 years, range 18 to 37 years) (Van Ginderdeuren 2011). All were productive daily and performed autogenic drainage for their airway clearance. The lung function of participants was not stated but some were noted to be on oxygen therapy. One participant withdrew after the first arm of the trial and therefore did not provide any cross‐over data that could be included in the analysis.
Interventions
One trial administered 4 mL of 6% hypertonic saline via an LC Star (PARI, Germany) nebuliser three times per day with the allocated timing regimen for that day (Dentice 2012). Hypertonic saline was nebulised immediately before or after airway clearance, or during airway clearance with blocks of inhalation and pauses for airway clearance. Participants using positive expiratory pressure (PEP) devices were not permitted to administer hypertonic saline simultaneously as this alters the inhaled dose and the distribution of the deposition (Laube 2005). The airway clearance technique was optimised for each participant on recruitment to the trial and was standardised for all three trial days. The second trial administered 4 mL of 6% hypertonic saline before or during 30 minutes of autogenic drainage (Van Ginderdeuren 2011).
The use of co‐interventions (such as bronchodilators and other inhaled medications) was not reported in the studies (Dentice 2012; Van Ginderdeuren 2011).
Outcomes measures
One trial measured the change in FEV₁ and FVC (in litres and percentage of the predicted value) recorded prior to and two hours following the middle treatment session of each trial day (Dentice 2012). Symptom scores at the end of each intervention arm were also recorded: perceived effectiveness; tolerability; and satisfaction rated on a 100‐mm visual analogue scale. Adverse events and adherence were also recorded. At the conclusion of the three‐day trial, participants reported their preferred timing regimen.
The second trial reported the change in dyspnoea scores at the conclusion of each intervention arm, wet weight of sputum in grams produced during the treatment session, and adverse events and adherence (Van Ginderdeuren 2011).
Excluded studies
Of the remaining 44 studies identified through our search strategy, two were excluded because they did not involve the administration of hypertonic saline at all. A further 41 studies were excluded because the interventions they compared did not differ in the timing of hypertonic saline inhalation (Excluded studies).
The remaining trial, published as an abstract only, is included within 'Studies awaiting classification' and will be further assessed when the full paper is published (O'Neil 2016).
Risk of bias in included studies
Please refer to Figure 1; Figure 2.

Risk of bias graph: review authors' judgements about each risk of bias item presented as percentages across all included studies.

Risk of bias summary: review authors' judgements about each risk of bias item for each included study.
Allocation
Generation of sequence
Both trials reported adequate methods of random generation of the allocation sequence: computer‐generated list (Dentice 2012) and allocations drawn from a box that had been shaken (Van Ginderdeuren 2011). Thus, the overall risk of bias due to the method of generation of the random sequence was low.
Concealment of allocation
Both trials reported using sealed opaque envelopes, so the overall risk of bias due to the non‐concealment of allocation was low.
Blinding
In both trials, participants were not blinded to the timing regimen, leading to a high risk of bias. In both trials, outcome assessors were blinded to the timing regimen, leading to a low risk of bias.
Incomplete outcome data
Both trials reported all available data. One trial stated no withdrawals occurred (Dentice 2012) and the other stated that one participant withdrew after the first arm of the trial and therefore did not provide any cross‐over data that could be included in the analysis (Van Ginderdeuren 2011) so analysis was conducted with all available data from 12 out of 13 participants (92%). Therefore, the overall risk of bias due to attrition was low.
Selective reporting
One trial was prospectively registered and remained consistent with this protocol (Dentice 2012). The second trial was not registered (Van Ginderdeuren 2011). The overall risk of bias was unclear.
Other potential sources of bias
No other potential sources of bias were identified.
Both of the trials met the external validity criterion of the PEDro score by stating both the source of participants and the eligibility criteria. Both trials met eight of the ten internal validity criteria on the PEDro score, with neither trial blinding participants or therapists.
Effects of interventions
Inhalation before versus during airway clearance techniques
Two studies with a total of 63 participants contributed data to this comparison (Dentice 2012; Van Ginderdeuren 2011).
Primary outcomes
1. Lung function
a. FEV₁
One trial provided data for this outcome (Dentice 2012). The change in FEV₁ from immediately before a treatment to two hours later was higher on average when hypertonic saline was inhaled before airway clearance techniques, with a MD of 0.04 litres (95% CI 0.00 to 0.08) (Analysis 1.1). However, this difference was not statistically significant when analysed using % predicted data (Analysis 1.2).
b. FVC
One trial provided data for this outcome (Dentice 2012). The change in FVC from immediately before a treatment to two hours later was not statistically significantly different between trial arms when analysed using data in litres (Analysis 1.3). However, change in FVC from immediately before a treatment to two hours later was higher on average when hypertonic saline was inhaled before airway clearance techniques when analysed using % predicted data, with a MD of 2.09% pred (95% CI 0.08 to 4.11) (Analysis 1.4).
2. Patient‐reported outcomes
a. QoL
No trial reported this outcome.
b. Symptom scores
Two studies with a total of 63 participants contributed data to this comparison (Dentice 2012; Van Ginderdeuren 2011), but the symptom scores used were different so no meta‐analysis was possible.
One trial provided data from 50 participants for perceived efficacy (i.e. ease of clearance), tolerability, and satisfaction, each recorded on a 10‐cm visual analogue scale (Dentice 2012). There were no significant differences in any of these outcomes when hypertonic saline was inhaled before versus during airway clearance techniques (Analysis 1.5; Analysis 1.6; Analysis 1.7).
The second trial provided data from 12 participants for dyspnoea severity (Van Ginderdeuren 2011). There was no significant difference in dyspnoea when hypertonic saline was inhaled before versus during airway clearance techniques (Analysis 1.8).
Secondary outcomes
1. Measures of sputum clearance
One trial provided data from 12 participants for wet weight of sputum (Van Ginderdeuren 2011). There was no significant difference in the wet weight of sputum when hypertonic saline was inhaled before versus during airway clearance techniques (Analysis 1.9).
2. Measures of exercise capacity
No trial reported this outcome.
3. Mortality
No trial reported this outcome.
4. Other pulmonary parameters
No trial reported any of the other pulmonary parameters listed in the protocol.
5. Frequency of exacerbations of respiratory infection
No trial reported this outcome.
6. Adherence to inhaled therapies, airway clearance techniques, and other therapies
There was 100% compliance with all the single doses of each treatment under supervision in both studies (Dentice 2012; Van Ginderdeuren 2011).
7. Adverse effects such as bronchospasm, cough and acute decline in pulmonary function
There were no adverse events in either trial (Dentice 2012; Van Ginderdeuren 2011).
Inhalation before versus after airway clearance techniques
One trial with 50 participants contributed data to this comparison (Dentice 2012).
Primary outcomes
1. Lung function (absolute change and change in per cent predicted if possible, otherwise final values)
a. FEV₁
The change in FEV₁ from immediately before a treatment to two hours later was not significantly influenced by whether hypertonic saline was inhaled before or after airway clearance techniques, whether analysed using data in litres (Analysis 2.1) or % predicted (Analysis 2.2).
b. FVC
The change in FVC from immediately before a treatment to two hours later was not significantly influenced by whether hypertonic saline was inhaled before or after airway clearance techniques, whether analysed using data in litres (Analysis 2.3) or % predicted (Analysis 2.4).
2. Patient‐reported outcomes
a. QoL
No trial reported this outcome.
b. Symptom scores
Perceived efficacy (i.e. ease of clearance) was rated statistically significantly better when hypertonic saline was inhaled before versus after airway clearance techniques, MD 10.62 mm (95% CI 2.54 to 18.70) (Analysis 2.5)
Tolerability was not rated significantly differently when hypertonic saline was inhaled before versus after airway clearance techniques (Analysis 2.6).
Satisfaction was rated significantly better when hypertonic saline was inhaled before versus after airway clearance techniques, MD 20.38 mm (95% CI 12.10 to 28.66) (Analysis 2.7).
Secondary outcomes
1. Measures of sputum clearance
No trial reported this outcome.
2. Measures of exercise capacity
No trial reported this outcome.
3. Mortality
No trial reported this outcome.
4. Other pulmonary parameters
No trial reported this outcome.
5. Frequency of exacerbations of respiratory infection
No trial reported this outcome.
6. Adherence to inhaled therapies, airway clearance techniques, and other therapies
There was 100% compliance with all the single doses of each treatment.
7. Adverse effects such as bronchospasm, cough and acute decline in pulmonary function
There were no adverse events in the trial.
Inhalation during versus after airway clearance techniques
One trial with 50 participants contributed data to this comparison (Dentice 2012).
Primary outcomes
1. Lung function
a. FEV₁
The change in FEV₁ from immediately before a treatment to two hours later was not significantly influenced by whether hypertonic saline was inhaled before or after airway clearance techniques, whether analysed using data in litres (Analysis 3.1) or % predicted (Analysis 3.2).
b. FVC
The change in FVC from immediately before a treatment to two hours later was not significantly influenced by whether hypertonic saline was inhaled before or after airway clearance techniques, whether analysed using data in litres (Analysis 3.3) or % predicted (Analysis 3.4).
2. Patient‐reported outcomes
a. QoL
No trial reported this outcome.
b. Symptom scores
Perceived efficacy (i.e. ease of clearance) was rated significantly better when hypertonic saline was inhaled during versus after airway clearance techniques, MD 15.60 mm (95% CI 17.55 to 23.65) (Analysis 3.5).
Tolerability was not rated significantly differently when hypertonic saline was inhaled during versus after airway clearance techniques (Analysis 3.6).
Satisfaction was rated significantly better when hypertonic saline was inhaled during versus after airway clearance techniques, MD 14.80 mm (95% CI 65.70 to 23.90) (Analysis 3.7).
Secondary outcomes
1. Measures of sputum clearance
No trial reported this outcome.
2. Measures of exercise capacity
No trial reported this outcome.
3. Mortality
No trial reported this outcome.
4. Other pulmonary parameters
No trial reported this outcome.
5. Frequency of exacerbations of respiratory infection
No trial reported this outcome.
6. Adherence to inhaled therapies, airway clearance techniques, and other therapies
There was 100% compliance with all the single doses of each treatment.
7. Adverse effects such as bronchospasm, cough and acute decline in pulmonary function
There were no adverse events in the trial.
Morning versus evening inhalation
No trial reported on this comparison.
Discusión
Resumen de los resultados principales
Las búsquedas identificaron 47 estudios, de los cuales dos estudios fueron elegibles para la inclusión ‐ proporcionando datos para 63 participantes. Los dos estudios usaron un diseño cruzado. Los períodos de intervención fueron cortos, de manera que los períodos de lavado de un día para otro probablemente fueron apropiados. Un ensayo administró tres tratamientos en un día para cada brazo del ensayo (Dentice 2012). El otro, un tratamiento único para cada brazo del ensayo en días separados (Van Ginderdeuren 2011).
No hubo diferencias clínicamente importantes entre los regímenes del momento adecuado antes, durante ni después de las técnicas de desobstrucción de las vías respiratorias en la cantidad media de mejoría en la función pulmonar, y las comparaciones entre los grupos no fueron significativas (Dentice 2012).
La eficacia percibida fue entre 10 y 20 mm inferior en una escala de 100 mm cuando la solución salina hipertónica se inhaló después de las técnicas físicas de desobstrucción de las vías respiratorias, en contraposición con antes o durante las técnicas (Dentice 2012). La tolerabilidad no fue afectada por el régimen del momento adecuado usado (Dentice 2012). No hubo diferencias significativas en la disnea ni el peso húmedo del esputo cuando la solución salina hipertónica se inhaló antes o durante las técnicas físicas de desobstrucción de las vías respiratorias (Van Ginderdeuren 2011). La satisfacción con todo el régimen de desobstrucción de las vías respiratorias fue significativamente inferior cuando la solución salina hipertónica se inhaló después de las técnicas físicas de desobstrucción de las vías respiratorias, en contraposición con antes o durante las técnicas (Dentice 2012).
Compleción y aplicabilidad general de las pruebas
No se encontró ningún ensayo que comparara la inhalación de solución salina hipertónica matutina versus vespertina. No se encontraron ensayos en poblaciones pediátricas. Por lo tanto, las recomendaciones de la revisión están limitadas al momento adecuado de la inhalación con relación a las técnicas de desobstrucción de las vías respiratorias en adultos.
Calidad de la evidencia
La mayoría de las posibles fuentes de sesgo se evaluaron como en riesgo bajo, excepto por el cegamiento ‐ ninguno de los ensayos incluidos cegó a los participantes ni a los terapeutas. A menudo es difícil para los ensayos de las intervenciones físicas lograr el cegamiento, aunque se logró en la mayoría de los ensayos en la revisión Cochrane del momento adecuado de la dornasa alfa (Dentice 2012) mediante un método de doble simulación. Es desalentador que ninguno de los ensayos incluidos utilizara este método para lograr el cegamiento.
Acuerdos y desacuerdos con otros estudios o revisiones
Aunque se encontraron dos ensayos elegibles que comparaban los regímenes del momento adecuado para la solución salina hipertónica con relación a las técnicas de desobstrucción de las vías respiratorias en adultos, ninguno de los resultados estaba presente en ambos ensayos. Por lo tanto, la interpretación de los datos debe reconocer que los resultados no se han repetido en estudios independientes. Sin embargo, uno de los estudios incluidos repitió la obtención de datos sobre 14 participantes en el plazo de un año luego de realizar el ensayo (Dentice 2012), con resultados muy similares a los datos originales obtenidos en los 50 participantes.
Los datos identificados por esta revisión apoyan el enfoque tradicional de la inhalación de solución salina hipertónica antes de las técnicas de desobstrucción de las vías respiratorias, como se ha usado en los estudios anteriores que demuestran la eficacia de la solución salina hipertónica para los pacientes con fibrosis quística (Elkins 2006c; Eng 1996; Robinson 1996; Robinson 1997). Sin embargo, los datos también indican que la inhalación durante la desobstrucción de las vías respiratorias puede ser igualmente efectiva.
Cuando se asesora acerca de la inhalación de solución salina hipertónica con relación al momento del día, ¿qué temas podrían considerarse a falta de las comparaciones directas de diferentes regímenes del momento adecuado de la inhalación de solución salina hipertónica? Los ensayos que demuestran la eficacia de la solución salina hipertónica regular han prescrito al menos dos dosis por día (Donaldson 2006; Elkins 2006c; Eng 1996). No se conoce el efecto de una única dosificación diaria sobre los resultados clínicos. Varios estudios indican que como se reduce la dosis de sal recibida, hay una reducción del efecto de la solución salina hipertónica sobre la reología del esputo (King 1997; Wills 1997), la limpieza mucociliar (Robinson 1997), y quizás algunos resultados clínicos (Elkins 2006d). Por lo tanto, se debe alentar a los individuos a recibir las dosis dos veces al día si son toleradas; sin embargo, para los que sólo toleran una dosis por día y optan por proseguir con este régimen, debe elegirse una alternativa acerca del momento adecuado durante el día. A falta de una comparación aleatoria de la inhalación matutina versus vespertina, podrían considerarse los factores individuales como la comodidad, el cumplimiento y la tolerabilidad. Por ejemplo, si un individuo tiene un calendario ajetreado por la mañana y tiempo libre después de las actividades del día, la inhalación vespertina puede ser más conveniente. Por el contrario, si los individuos observan mayor tos por la noche y trastornos del sueño con la inhalación vespertina, la inhalación matutina podría ser mejor tolerada.

Risk of bias graph: review authors' judgements about each risk of bias item presented as percentages across all included studies.

Risk of bias summary: review authors' judgements about each risk of bias item for each included study.

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 1 FEV1 (L).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 2 FEV1 (% pred).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 3 FVC (L).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 4 FVC (% pred).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 5 Perceived efficacy (mm).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 6 Tolerability (mm).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 7 Satisfaction (mm).

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 8 Dyspnoea.

Comparison 1 Inhalation before versus during airway clearance techniques, Outcome 9 Sputum wet weight.

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 1 FEV1 (L).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 2 FEV1 (% pred).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 3 FVC (L).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 4 FVC (% pred).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 5 Perceived efficacy (mm).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 6 Tolerability (mm).

Comparison 2 Inhalation before versus after airway clearance techniques, Outcome 7 Satisfaction (mm).

Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 1 FEV1 (L).
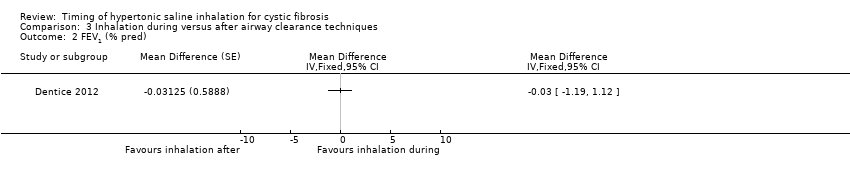
Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 2 FEV1 (% pred).

Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 3 FVC (L).

Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 4 FVC (% pred).
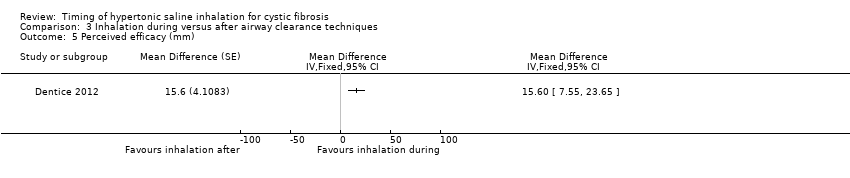
Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 5 Perceived efficacy (mm).

Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 6 Tolerability (mm).

Comparison 3 Inhalation during versus after airway clearance techniques, Outcome 7 Satisfaction (mm).
| Outcome or subgroup title | No. of studies | No. of participants | Statistical method | Effect size |
| 1 FEV1 (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 2 FEV1 (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 3 FVC (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 4 FVC (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 5 Perceived efficacy (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 6 Tolerability (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 7 Satisfaction (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 8 Dyspnoea Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 9 Sputum wet weight Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| Outcome or subgroup title | No. of studies | No. of participants | Statistical method | Effect size |
| 1 FEV1 (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 2 FEV1 (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 3 FVC (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 4 FVC (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 5 Perceived efficacy (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 6 Tolerability (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 7 Satisfaction (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| Outcome or subgroup title | No. of studies | No. of participants | Statistical method | Effect size |
| 1 FEV1 (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 2 FEV1 (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 3 FVC (L) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 4 FVC (% pred) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 5 Perceived efficacy (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 6 Tolerability (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |
| 7 Satisfaction (mm) Show forest plot | 1 | Mean Difference (Fixed, 95% CI) | Totals not selected | |

